某混合溶液中可能含有的离子如下表所示:
| 可能大量含有的阳离子 |
H+、Ag+、Mg2+、Al3+、NH4+、Fe3+ |
| 可能大量含有的阴离子 |
Cl-、Br-、I-、CO32—、AlO2— |
为探究其成分,进行了以下探究实验。
(1)探究一:
甲同学取一定量的混合溶液,向其中逐滴加入氢氧化钠溶液,产生沉淀的物质的量(n)与加入氢氧化钠溶液的体积(V)的关系如图所示。
①该溶液中一定不存在的阳离子是 ,
一定不存在的阴离子是 ;含有的阳离子其对应物质的量浓度之比为 ;
②请写出沉淀减少过程中发生反应的离子方程式 。
(2)探究二:
乙同学检测到该溶液中含有大量的Cl-、Br-、I-,若向1 L该混合溶液中通入一定量的Cl2,溶液中Cl-、Br-、I-的物质的量与通入Cl2的体积(标准状况)的关系如下表所示,分析后回答下列问题:
| Cl2的体积(标准状况) |
11.2 L |
22.4 L |
28.0 L |
| n(Cl-) |
2.5 mol |
3.5 mol |
4.0 mol |
| n(Br-) |
3.0 mol |
2.5 mol |
2.0 mol |
| n(I-) |
x mol |
0 |
0 |
①当起始至通入Cl2的体积为22.4 L时,溶液中发生反应总的离子方程式为 ;
②原溶液中Cl-、Br-、I-的物质的量浓度之比为 。
一种由电石跟水反应制得的烃,经合成可得C4H4的烃,它是合成一种橡胶的中间体,它有多种同分异构体。
(1)试写出它的一种链式结构的异构体的结构简式________。
(2)它有一种同分异构体,每个碳均达饱和,且构成的空间构型中碳与碳的夹角都相同,该分子中碳原子形成的空间构型呈________型。
根据要求写出名称或结构简式:
(1)
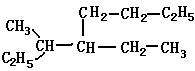 名称:
名称:
(2)3-甲基-1-丁烯结构简式:
(3)2,2,4—三甲基戊烷结构简式:
下列物质中,互为同系 物的是,互为同分异构体的是,互为同素异形体的是。(填入代号)
物的是,互为同分异构体的是,互为同素异形体的是。(填入代号)
⑴苯⑵石墨⑶2—甲基丁烷⑷氕⑸C6H5—CH3⑹金刚石
⑺氘⑻氯仿⑼氚⑽三氯甲烷⑾新戊烷
已知:
A与芳香族化合物B在一定条件下反生成C,进一步反应生成抗氧化剂阿魏酸(见下图)
A的相对分子质量是104,1molA与足量NaHCO3溶液反应生成2mol气体。
(1)A的结构简式是________________。
(2)在中学学过知识里 B不可能发生的反应是________ (填序号)
a、取代反应 b、加成反应c、氧化反应d、 还原反应e、水解反应 f、显色反应
(3)等物质的量C分别与足量的Na、浓溴水、NaOH、NaHCO3反应时消耗Na、Br2、NaOH、NaHCO3的物质的量之比是________________
(4)写出C与足量的Na2CO3的化学方程式为: _____________________________________
(5)写出符合下列条件的阿魏酸所有的同分异构体的结构简式:。
①在苯环上只有两个取代基;
②在苯环上的一氯取代物只有两种;
③1mol该同分异构体与足量NaHCO3反应生成2mol CO2气体;
④该同分异构体进行核磁共振氢谱分析发现只有4种峰。
(6)写出利用阿魏酸在一定条件下生成抗氧化性的高分子化合物的方程式:
___________________________________________________________________________。
已知和碳元素同主族的X元素位于周期表中的第一长周期,短周期元素Y原子的最外层电子数比内层电子总数少3,它们所形成化合物的分子式是XY4。试回答:
(1)X元素的原子基态时电子排布式为;Y元素原子最外层电子的轨道表示式为。
(2)若X、Y两元素电负性分别为1.8和3.0,则XY4中X与Y之间的化学键为(填“共价键”或“离子键”)。
(3)该化合物的空间结构为,中心原子的杂化类型为,分子为(填“极性分子”或“非极性分子”)。
(4)该化合物在常温下为液体,该化合物中分子间作用力是。
(5)该化合物的沸点与SiCl4比较,(填化学式)的较高,原因是。