下列各组离子能在指定溶液中大量共存的是
①无色溶液中:
②常温下,pH=14的溶液中:
③室温下水电离的
④加入Mg能放出H2的溶液中:
⑤使甲基橙变红的溶液中:
⑥室温下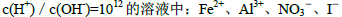
| A.①③⑥ | B.①②⑤ | C.②④⑤ | D.①③④ |
下表是部分短周期元素的原子半径及主要化合价,根据表中信息,判断以下叙述正确的是
| 元素代号 |
L |
M |
Q |
R |
T |
| 原子半径/nm |
0.160 |
0.134 |
0.089 |
0.102 |
0.074 |
| 主要化合价 |
+2 |
+3 |
+2 |
+6、-2 |
-2 |
A.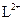 与 与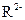 的核外电子数相等 的核外电子数相等 |
B.L与T形成的化合物具有两性 |
C.氢化物的稳定性为 |
D.单质与浓度相等的稀盐酸反应的速率为Q<L |
下列叙述中,金属a的活泼性肯定比金属b的活泼性强的是
A.a原子的最外层电子数比B原子的最外层电子数少
B.常温时,a能从水中置换出氢,而b不能
C 1mol a从酸中置换H+生成的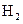 比l mol b从酸中置换
比l mol b从酸中置换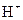 生成的
生成的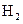 多
多
D.a原子电子层数比b原子的电子层数多
将mg块状碳酸钙跟足量盐酸反应,反应物损失的质量随时间的变化曲线如下图的实线所示,在相同的条件下,将mg粉末状碳酸钙与同浓度足量盐酸反应,则相应的曲线(图中虚线所示)正确的是
在期表主族元素中,甲元素与乙、丙、丁三元素相邻,甲、乙的原子序数之和等于丙的原子序数;这四种元素原子的最外层电子数之和为20。下列判断中,正确的是
| A.气态氢化物的稳定性:甲>丙 |
| B.原子半径:丙>乙>甲>丁 |
| C.最高价氧化物对应水化物的酸性:丁>甲 |
| D.乙和甲或乙和丁所能形成的化合物都是有毒物质 |
下列化学用语书写正确的是
| A.氮气分子的结构式::N≡N: | B.高氯酸的分子式: |
C.氯化镁的电子式: |
D.氯化氢的电子式: |