金属钛(Ti)性能优越,被称为继铁、铝之后的“第三金属”。工业上以金红石为原料制取Ti的反应为
(1)aTiO2+bCl2+cC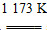 aTiCl4+cCO
aTiCl4+cCO
(2)TiCl4+2Mg Ti+2MgCl2
Ti+2MgCl2
关于反应(1)、(2)的分析不正确的是
①TiCl4在反应(1)中是还原产物,在反应(2)中是氧化剂
②C、Mg在反应中均为还原剂,发生还原反应 ③每生成19.2 g Ti,反应(1)、(2)中共转移4.8 mol e- ④a=1,b=c=2
A.①②④ B.②③④ C.③④ D.②③
化学与科学、技术、社会、环境密切相关,下列叙述正确的是
| A.目前科学家已经制得单原子层锗,其电子迁移率是硅的10倍,有望取代硅用于制造更好的晶体管 |
| B.石油裂解的主要目的是提高汽油等轻质油的产量与质量,石油催化裂化的主要目的是得到更多的乙烯、丙烯等气态短链烃 |
| C.汽车尾气催化转化装置可将尾气中的NO和CO等有害气体转化为N2和CO2,该装置中的催化剂可降低NO和CO反应的活化能,有利于提高该反应的平衡转化率 |
| D.近期在西非国家爆发的埃博拉疫情呈加速蔓延之势,已知该病毒对化学药品敏感,乙醇、次氯酸钠溶液均可以将病毒氧化而达到消毒的目的 |
【原创】常温下,下列有关叙述正确的是
A.水的离子积KW只与温度有关,但水的电离程度一定会受外加酸、碱、盐的影响
B.若HA的Ka=1.7×10—5,BOH的Kb=1.7×10—5,则HA溶液中的c(H+)与BOH中的c(OH-)相等
C.将0.2mol/L HA溶液和0.1mol/L NaOH溶液等体积混合,则反应后的混合液中:c(OH—)+ c(A—) =c(H+)+ c(HA)
D.Mg(OH)2能溶于NH4Cl浓溶液的主要原因是NH4+结合OH—使沉淀溶解平衡发生移动
【改编】在一定条件下的恒容密闭容器中发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),图1表示反应过程中能量的变化,图2表示反应过程中物质浓度的变化。下列有关说法正确的是
CH3OH(g)+H2O(g),图1表示反应过程中能量的变化,图2表示反应过程中物质浓度的变化。下列有关说法正确的是
| A.该反应在高温下才能自发进行 |
| B.再加入一定量CO2,则n(CH3OH)/n(CO2)增大 |
C.温度降低,CH3OH(g)+H2O(g) CO2(g)+3H2(g)的平衡常数K增大 CO2(g)+3H2(g)的平衡常数K增大 |
| D.从反应开始到平衡,用氢气表示的平均反应速率为0.225 mol/(L·min) |
【原创】下列实验装置图正确的是
【改编】已知A、B、C、D之间的转化关系为:A + B → C + D,则下列有关说法不正确的是
A.若A为Fe,D为氢气,则B可能是酸,也可能是水
B.若B为水,D为氧气,则A可能是单质,也可能是化合物
C.若A、B、C、D均为化合物,该反应可能是复分解反应,也可能是氧化还原反应
D.若A、B、C、D均为10电子微粒,且C是水,则D一定能使湿润的红色石蕊试纸变蓝