下列说法正确的是( )
| A.原子核外电子层数越多,原子半径越大 |
| B.每一主族所含非金属元素的种类可表示为︳族序数-2 |
C.根据泡利原理将氧元素基态原子的电子排布图书写为 |
| D.C2H2分子中的碳采取sp2杂化 |
下列说法错误的是
①NaHCO3溶液加水稀释,c(Na+)/c(HCO3-)的比值保持增大
②浓度均为0.1 mol/L的Na2CO3、NaHCO3混合溶液:2c(Na+)=3[c(CO32-)+c(HCO3-)]
③在0.1 mol/L氨水中滴加0.l mol/L盐酸,恰好完全中和时溶液的pH=a,则由水电离产生的c(OH-)=l0-a mol/L
④向0.1mol/LNa2SO3溶液中加入少量NaOH固体,c(Na+)、c(SO32-)均增大
⑤在Na2S稀溶液中,c(H+)=c(OH-)+c(H2S)+c(HS-)
| A.①④ | B.②④ | C.①③ | D.②⑤ |
下列装置进行的相应实验,能达到实验目的的是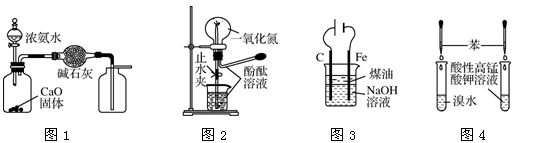
| A.用图1装置制取并收集干燥纯净的NH3 |
| B.用图2装置可演示NO的喷泉实验 |
| C.用图3装置制备Fe(OH)2并能较长时间观察其颜色 |
| D.用图4装置验证苯中是否有独立的碳碳双键 |
下列说法正确的是
| A.根据反应3Fe+8HNO3=3Fe(NO3)2+2NO↑+4H2O可知:反应中HNO3表现酸性和氧化性 |
| B.根据反应H3PO3+2NaOH(足量)=Na2HPO3+2H2O可知:H3PO3属于三元酸 |
| C.根据反应5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O可知:用酸性KMnO4溶液可检验绿矾(FeSO4·7H2O)是否变质 |
| D.根据反应CuSO4+H2S=CuS↓+H2SO4可知:H2S的酸性比H2SO4强 |
设NA为阿伏加德罗常数的值。下列叙述正确的是
| A.标准状况下,11.2 L SO3所含的氧原子数为1.5NA |
| B.电解精炼铜时,若阳极质量减少6.4 g,则电路中转移电子数为0.2NA |
| C.常温常压下,4.0 g CH4中含有共价键的数目为NA |
| D.在含Al3+总数为NA的AlCl3溶液中,Cl-总数为3NA |
分子式为C5H10O2的羧酸和酯,且有3个甲基的同分异构体共有(不考虑立体异构)
| A.3种 | B.4种 | C.5种 | D.6种 |