某校同学为探究Br2、I2和Fe3+的氧化性强弱,进行了如下实验。
实验①:取少量KI溶液于试管中,先加入溴水、振荡,再加入CCl4,振荡后静置,观察到下层液体呈紫红色;
实验②:取少量FeSO4溶液于试管中,先加入溴水,振荡,再继续滴加两滴KSCN溶液,振荡,观察到溶液呈红色。
(1)写出离子方程式:
实验①:______________________________________________________;
实验②:______________________________________________________。
(2)由上述两个实验,对物质的氧化性可以得出的正确结论是________。
| A.Br2>I2 | B.Fe3+>Br2 | C.Br2>Fe3+ | D.I->Br- |
(3)已知Fe3+的氧化性强于I2,请你从所给试剂中选择所需试剂,设计一个实验加以证明。(提示:请写出实验步骤、现象及结论)
①FeCl3溶液 ②碘水 ③KI溶液 ④稀H2SO4 ⑤淀粉溶液
以钛酸亚铁(FeTiO3)为原料制取BaTiO3的过程如下图所示:
(1)FeTiO3与稀硫酸反应,产物有TiOSO4、H2O和(填化学式)。
(2)已知:TiO2(s)+H2SO4(aq)=TiOSO4(aq)+H2O (l) △H=akJ·mol-1
H2TiO3(s)=TiO2(s)+H2O (l) △H=b kJ·mol-1
写出TiOSO4水解生成H2TiO3的热化学方程式。
(3)写出TiO2生成BaTiO3的化学方程式。
4种短周期元素相对位置如下表。M元素既是构成生物体的基本元素,又是构成地壳中岩石和化石燃料的主要元素。回答下列问题:
(1)X的原子结构示意图为。
(2)0.1 molQ的10电子氢化物与CuO反应生成Cu2O、H2O和Q单质时,生成Cu2O的物质的量是。
(3)Y的氧化物与NaOH溶液反应的化学方程式是。
(4)HR是含M元素的一元酸。常温下,0.1 mol·L-1 HR溶液中,c(H+)=1.3×10-3 mol·L-1。则HR H++R-的电离平衡常数Ka=(保留一位小数)。
H++R-的电离平衡常数Ka=(保留一位小数)。
用如图所示装置做“铜与浓硝酸反应”的实验。
(1)从试剂瓶中取出一小块铜片放入试管中,需用的仪器是。
(2)棉花应蘸溶液(填化学式)。
(3)试管中除了溶液变成绿色外,还会出现的现象是(填序号)。
A.有红棕色气体生成,上下颜色相同
B.有红棕色气体生成,上部颜色较浅
C.有红棕色气体生成,下部颜色较浅
(4)实验结束后,对试管内残留物的处理方法是。
向含2 mol H2SO4和1 mol HNO3的混合稀溶液中加入过量的锌,假设HNO3被还原的产物全部为NO。
①写出反应的离子方程式。
②生成的气体在标况下的体积为:。
金属及其化合物在人类生活、生产中发挥着重要的作用。
(1)钠、铝、铁三种金属元素所形成的各种氧化物中具有强氧化性的是(填化学式,下同);适宜做耐火材料的是。
(2)若Na2CO3粉末中混有少量NaHCO3杂质,最适宜的除杂方法是,反应的化学方程式为。
(3)要除去铁粉中混有的少量铝粉,适宜的试剂是,发生反应的离子方程式为。
(4)取少量FeCl2溶液,按下图所示操作,使其跟NaOH溶液反应。可观察到的实验现象是。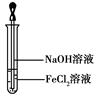
(5)向盛有氯化铁、氯化亚铁、氯化铜混合溶液的烧杯中加入铁粉和铜粉,反应结束后,下列结果不可能出现的是(填序号)。
| A.有铜无铁 | B.有铁无铜 | C.铁、铜都有 | D.铁、铜都无 |