绿原酸的结构简式如图所示下列有关绿原酸的说法不正确的是( )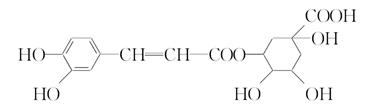
| A.分子式为C16H18O9 |
| B.能与Na2CO3反应 |
| C.能发生取代反应和消去反应 |
| D.0.1 mol绿原酸最多与0.8 mol NaOH反应 |
湿润的KI-淀粉试纸接触某气体而显蓝色,该气体中可能是()
①Cl2②NO2③H2S④SO2⑤HCl⑥溴蒸气
| A.①③④ | B.①②⑤ | C.①②⑥ | D.②④⑤ |
为确定下列置于空气中的物质是否变质,所选检验试剂(括号内物质)不能达到目的的是()
| A.Na2SO3溶液(BaCl2) | B.FeCl2溶液(KSCN) |
| C.KI(淀粉溶液) | D.HCHO溶液(石蕊试液) |
用分液漏斗可以分离的一组混合物是()
| A.溴苯和水 | B.乙酸乙酯和乙酸 | C.溴乙烷和乙醇 | D.乙醇和水 |
下列说法正确的是
| A.苯酚、硫氰化钾、乙酸、氢氧化钾四种溶液可用FeCl3溶液一次鉴别() |
| B.CH3CH2OH、CH2=CHCOOH、CH3CHO、CH3COOH四种溶液可用新制Cu(OH)2一次鉴别 |
| C.除去KCl溶液中的少量MgCl2:加入适量的NaOH溶液,过滤 |
| D.KCl溶液中混有少量KI,可通入足量Cl2后,再用乙醇进行萃取、分液 |
下列各组稀溶液,不用其它试剂或试纸,仅利用溶液间的相互反应,不能将它们区别开的是()
| A.KNO3、Na2SO4、CaCl2、BaCl2 | B.NaHSO4、MgSO4、Na2CO3、NaOH |
| C.HCl、BaCl2、Na2CO3、NaOH | D.H2SO4、Al2(SO4)3、NaCl、NaOH |