用NA表示阿伏加德罗常数的值。下列叙述中一定正确的是( )
| A.一定条件下4.6 g Na完全与O2反应生成7.2 g产物,失去的电子数为0.2NA |
| B.50 mL 18.4 mol/L浓硫酸与足量铜加热反应,生成SO2的分子数为0.46NA |
| C.一定条件下某密闭容器盛有0.1 mol N2和0.3 mol H2,充分反应后转移电子数为0.6NA |
| D.电解1 L NaCl溶液至c(OH-)="0.2" mol/L,转移电子数为0.4NA |
下列实验操作先后顺序正确的是
| A.先装好药品,后检查装置的气密性 |
| B.先用双手握紧试管,后将导管插入水中以检查装置的气密性 |
| C.用排水集气法集满气体后,先熄灭酒精灯,后撤导气管 |
| D.结束碳酸氢钠热稳定性的实验时,先撤导气管,后熄灭酒精灯 |
关于容量瓶的使用,下列操作正确的是
| A.使用前要检验容量瓶是否漏液 |
| B.用蒸馏水荡洗后必须要将容量瓶烘干 |
| C.为了便于操作,浓溶液稀释或固体溶解可直接在容量瓶中进行 |
| D.为了使所配溶液浓度均匀,定容结束后,手握瓶颈,左右振荡 |
下列物质中,能够导电的电解质是
| A.Cu丝 | B.熔融的MgCl2 |
| C.NaCl溶液 | D.蔗糖 |
氧化还原反应的实质是
| A.氧元素的得与失 | B.化合价的升降 |
| C.电子的得失或偏移 | D.分子中原子重新组合 |
25℃,有c(CH3COOH)+c(CH3COO-)=0.1mol·L-1的一组醋酸和醋酸钠混合溶液,溶液中c(CH3COOH)、c(CH3COO-)与pH值的关系如图所示。下列有关离子浓度关系叙述正确的是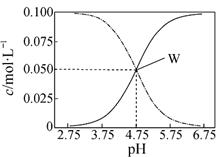
| A.pH=5.5溶液中:c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-) |
| B.W点表示溶液中:c(Na+)=c(CH3COO-)+c(CH3COOH) |
| C.pH=3.5溶液中:c(Na+)+c(H+)-c(OH-)+c(CH3COOH)=0.1mol·L-1 |
| D.向W点所表示的1.0L溶液中通入0.05molHCl气体(溶液体积变化可忽略): |
c(H+)=c(CH3COOH)+c(OH-)