下列有关的离子方程式中正确的是( )
| A.氯化铝溶液中加入过量氨水:Al3++4NH3·H2O=AlO2—+4NH4++2H2O |
B.铜片接电源正极,碳棒接电源负极,电解硫酸溶液:Cu+2H+ Cu2++H2↑ Cu2++H2↑ |
C.磷酸一氢钠溶液水解:HPO42—+H2O PO43—+H3O+ PO43—+H3O+ |
| D.实验室配制的亚铁盐溶液在空气中被氧化:4Fe2++O2+2H2O=4Fe3++4OH- |
根据键能数据估算Si(s)+O2 (g)=SiO2(s)的反应热ΔH为 ()
| 化学键 |
Si—O |
Si-Si |
O=O |
Si-C |
| 键能/(kJ/mol) |
460 |
176 |
498 |
155[ |
A.–246 kJ · mol-1 B.+246 kJ · mol-1 C.–990 kJ · mol-1 D.+990 kJ · mol-1
下列叙述正确的是()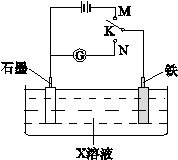
| A.K与N连接时,X为硫酸,一段时间后溶液的pH增大 |
| B.K与M连接时,X为硫酸,一段时间后溶液的pH增大 |
| C.K与N连接时,X为氯化钠,石墨电极上的反应为:2H++2e—=H2↑ |
| D.K与M连接时,X为氯化钠,石墨电极上的反应为:4OH—-4e—=2H2O+O2↑ |
下列有关金属的腐蚀与防护的说法不正确的是()
| A.地下钢管连接镁块可以保护地下钢管 |
| B.纯银制品在空气中因化学腐蚀渐渐变暗 |
| C.当镀锌铁制品的镀层破损时,镀层不能对铁制品起保护作用 |
| D.水中的钢闸门连接电源的负极可以保护钢闸门 |
长式周期表共有18个纵行,从左到右排为1—18列,即碱金属为第一列,稀有气体元素为第18列。按这种规定,下列说法正确的是 ()
| A.s区元素都是金属元素 | B.第13列的元素原子最外层电子排布为ns2 np1 |
| C.第四周期第9列元素是铁元素 | D.第10、11列为ds区 |
下列化学用语说法正确的是( )
A.过氧化钠的电子式: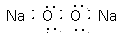 |
B.钾元素的原子结构示意图为:K  |
| C.次氯酸的结构式: H-O-Cl |
D.硫原子的电子排布图为: |
1s 2s 2p 3s 3p