氨的催化氧化过程主要有以下两个反应:
(ⅰ)4NH3(g)+5O2(g) 4NO(g)+6H2O(g) ΔH=-905.5 kJ·mol-1
4NO(g)+6H2O(g) ΔH=-905.5 kJ·mol-1
(ⅱ)4NH3(g)+3O2(g) 2N2(g)+6H2O(g) ΔH=-1267 kJ·mol-1
2N2(g)+6H2O(g) ΔH=-1267 kJ·mol-1
测得温度对NO、N2产率的影响如图所示。下列说法错误的是( )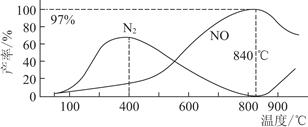
| A.升高温度,反应(ⅰ)和(ⅱ)的平衡常数均减小 |
| B.840 ℃后升高温度,反应(ⅰ)的正反应速率减小,反应(ⅱ)的正反应速率增大 |
| C.900 ℃后,NO产率下降的主要原因是反应(ⅰ)平衡逆向移动 |
| D.800 ℃左右时,氨的催化氧化主要按照(ⅰ)进行 |
下列各组物质沸点大小关系正确的是()
①CH3CH2CH2OH > CH3(CH2)2CH3② CH3(CH2)2CH3 > CH3CH(CH3)2
③苯酚>苯 ④ CH3CH2Br > CH3CH2OH⑤
| A.①④ | B.②④⑤ | C.①②③ | D.③④⑤ |
已知298K时,Ksp(CaCO3)= 2.80×10-9,Ksp(CaSO4)= 4.90×10-5。若用难溶盐在溶液中的物质的量浓度来表示其溶解度,则下面的叙述正确的是( )
| A.298K时,CaSO4的溶解度约为7.00×10-2 mol/L |
| B.反应CaSO4(s) + CO32-= CaCO3(s) + SO42-在298K时的平衡常数K= Ksp(CaSO4) / Ksp(CaCO3) = 1.75×104 |
| C.CaCO3、CaSO4的饱和溶液的导电能力很弱,所以它们都是弱电解质 |
| D.升高温度,两种盐的溶度积与溶解度都保持不变 |
下列各组中两个反应的类型相同的是()
| A.苯转化为溴苯、苯酚转化为环己醇 |
| B.由乙醇制溴乙烷、由乙烯制溴乙烷 |
| C.乙烯使溴水褪色、乙醇使酸性重铬酸钾溶液变为蓝绿色 |
| D.由乙炔制氯乙烯、由氯乙烯制聚氯乙烯 |
某链状有机物分子中含m个 ,n个-C2H5, a个
,n个-C2H5, a个 其余为氯原子,则氯原子的数目可能是()
其余为氯原子,则氯原子的数目可能是()
| A.m+2-n | B.n+2a-3m |
| C.n+m+a | D.a+n+2-2m |
棉籽中可以提取出一种叫做棉酚的物质,具有抗癌作用,其市场价格相当于黄金价格的60倍。棉酚的结构如右图所示,下列关于棉酚的说法不正确的是()
| A.棉酚放置在空气中容易变质 |
| B.用核磁共振氢谱可以证明棉酚分子中有9种氢原子 |
| C.棉酚完全燃烧产生的CO2的物质的量是H2O的2倍 |
| D.棉酚能与NaOH溶液、溴水发生反应 |