铁是人类必需的微量元素之一,它可以促进血红蛋白结合氧分子进行输氧,医学上经常用硫酸亚铁糖衣片给患贫血的病人补铁.请根据以下药品说明书回答问题:
(1)药片上的糖衣可以起__________的作用,鉴定时溶解加盐酸的目的是____________。
(2)某研究小组甲欲用KMnO4测定FeSO4的含量。
①实验前,首先要精确配制一定物质的量浓度的KMnO4溶液250毫升,配制时需要的仪器除托盘天平、烧杯、玻璃棒、量筒外,还需要的仪器有__________、___________。
②滴定时含硫酸亚铁的滤液放在___________(填仪器)中,高锰酸钾溶液放在__________(填仪器)中,滴定时加入___________(填“酚酞”或“甲基橙”或“石蕊”或“不用加”)指示剂,如何判断达到滴定终点_____________。
(3)另一研究小组乙设计了如下测量方案: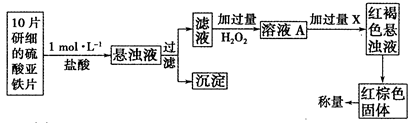
①此检验过程中加过量H2O2反应的离子方程式为______________。
②从红褐色的悬浊液到最后的称量,其过程中所需的基本操作有___________(按操作的顺序填写)。
| A.过滤 | B.洗涤 | C.萃取 | D.分液 E.冷却 F.灼烧 |
③最后称量红棕色固体的质量为0.8960g,那么该药片中硫酸亚铁的质量分数为_________(小数点后面保留一位有效数字)。
为探究Fe(NO3)2等硝酸盐热分解产物和产物的性质,某化学小组开展如下探究性学习:
【查阅资料】金属活泼性不同,其硝酸盐分解产物不同
(1)K→Na活泼金属的硝酸盐分解生成亚硝酸盐和氧气;
(2)Mg→Cu等较活泼金属的硝酸盐分解生成氧化物、NO2和O2;
(3)Hg以后不活泼金属的硝酸盐分解生成金属、NO2和O2。
2KNO3 2KNO2↑+O2↑ 2Cu(NO3)2
2KNO2↑+O2↑ 2Cu(NO3)2 2CuO+4NO2↑+O2↑
2CuO+4NO2↑+O2↑
2AgNO3 2Ag+2NO2↑+O2↑
2Ag+2NO2↑+O2↑
I:【实验一】探究Fe(NO3)2热分解固体产物中Fe元素的价态。该小组甲同学将其溶于足量的稀H2SO4得到相应两份溶液,进行以下探究实验。①向一份溶液中滴入少量KSCN溶液;②少量稀酸性KMnO4溶液中滴入另一份溶液。现象:①溶液变红色;②溶液变红色。
(1)则Fe(NO3)2分解的化学方程式是 。
II:【实验二】探究Fe(NO3)2热分解气体产物的性质。小组乙、丙同学进行了如下图所示的实验(收集时操作恰当,几乎没有空气)
实验步骤:①连接仪器;②检查装置气密性;③取一定质量Fe(NO3)2装于大试管,并重新连接好仪器;④加热;⑤……
(2)乙同学使用A装置收集气体,恰好收集到54mL红棕色气体,要从水槽中取出量筒,乙同学的正确操作方法是 。
(3)丙同学取等质量Fe(NO3)2的在同样条件下热分解,用B装置收集气体产物,可收集到气体_____mL。
III:【实验三】探究固体混合物的组成和特征
(4)小组丁同学取KNO3、 Cu(NO3)2、 Fe(NO3)2混合粉末充分加热后用排水法未收集到任何气体,则KNO3、Cu(NO3)2、 Fe(NO3)2物质的量之比可能为____________。
| A.1∶2∶2 | B.2∶1∶3 | C.1∶2∶3 | D.3∶8∶5 |
(5)取0.6mol由KNO3、 Cu(NO3)2、 Fe(NO3)3按等物质的量之比混合而成的粉末溶于100mL 3mol/L的稀硫酸中,再向溶液中加入足量的铜粉,则最多可溶解铜粉质量为_________
某同学用图示装置进行铁与稀硝酸反应的实验并进行相关的实验探究。(共计13分)
实验步骤:
a.向广口瓶内注入足量热NaOH溶液,将盛有一定质量的
纯铁粉的小烧杯放入瓶中。
b.关闭止水夹,点燃红磷,伸入瓶中,塞好橡胶塞。
c.待红磷充分燃烧,一段时间后打开分液漏斗旋塞,向小
烧杯中滴入一定量的4mol/L的稀硝酸,铁粉完全溶解。
(一)气体产物成分探究
(1)实验前如何检查该装置的气密性?
(2)燃烧红磷的目的是
(3)为证明气体产物为NO,步骤c后还缺少的一步主要操作是 。
(二)产物中铁元素价态探究
(1)提出合理假设
假设1:产物中只有+2价铁元素;假设2: ;
假设3:产物中既有+2价铁元素,又有+3价铁元素.
(2)设计实验方案,证明假设1成立(写出实验操作步骤、现象和结论): 。
(三)问题讨论
(1)广口瓶中热NaOH溶液的主要作用是 。
(2)若假设3成立,且所得溶液中n(Fe2+)︰n(Fe3+)=3︰1时,则相应反应的离子方程式为 。
氢化钙(CaH2)固体是一种储氢材料,是登山运动员常用的能源提供剂。某化学小组的同学在老师的指导下制备氢化钙。
【查阅资料】
氢化钙通常用氢气与钙加热制得。
氢化钙要密封保存,遇水反应生成氢氧化钙和氢气。
钙遇水立即发生剧烈反应生成氢氧化钙和氢气,并放出大量的热。
标准状况下氢气的密度为0.09g/L。
【进行实验】小组同学设计的制取装置如下图所示(固定装置略)。
回答下列问题:
(1)写出A中发生反应的化学方程式 。
(2)B、D中所盛试剂相同,该试剂为 ,其作用分别是 、 。
(3)实验时先打开A中活塞,一段时间后,再点燃C中酒精灯,其目的是 。
(4)装置C中制取氢化钙的化学方程式是 。
【实验反思】小组同学通过反思提出问题:上述制得的氢化钙是否纯净?
他们再次设计实验进行检验,实验步骤如下:
步骤1:检查装置气密性,装入足量的水和已称好质量的氢化钙样品,按图所示连接仪器(固定装置略).
步骤2:将Y形管倾斜,使A中的水全部进入B中,完全反应后,冷却至室温,读取量筒读数.
通过上述实验可分析出制得的氢化钙是否纯净,其依据是______.
某兴趣小组的同学发现将一定量的铁与浓硫酸加热时,观察到铁完全溶解,并产生大量气体。为此,他们设计了如下装置验证所产生的气体。
(1)填写装置的作用:B ,C ,G ,
(2)证明有SO2生成的现象是
(3)可以证明气体X中含有氢气的实验现象是:E中:_____________,F中:__________。如果去掉装置D,还能否根据F中的现象判断气体中有氢气?________(填“能”或“不能”),原因是_________。
(4)反应后A的溶液中含有Fe3+和Fe2+,检验其中的Fe2+的方法是 。
(5)若将铁丝换成铜丝,反应后的溶液没有出现预计的蓝色溶液,而出现了大量白色固体,原因是 ,要确认CuSO4生成,待试管冷却后, 。
取6根铁钉,6支干净的试管及其他材料,如图所示。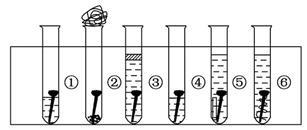
试管①放入一根铁钉,再注入蒸馏水,使铁钉和空气及水接触;
试管②在试管底部放入硅胶(是一种干燥剂),再放入铁钉,用棉花团堵住试管口,使铁钉和干燥空气接触;
试管③先放入一根铁钉,趁热倒入煮沸的蒸馏水(已赶出原先溶解在蒸馏水中的空气)浸没铁钉,再加上一层植物油,使铁钉不能跟空气接触;
试管④中放入铁钉注入食盐水,使铁钉和空气及食盐水接触;
试管⑤放入相连的铁钉和锌片,注入自来水,浸没铁钉和锌片;
试管⑥放入相连的铁钉和铜丝,注入自来水,浸没铁钉和铜丝。
把6支试管放在试管架上,几天后观察铁钉被腐蚀的情况。
(1)上述实验中铁钉发生了电化学腐蚀的是______ (填试管序号);在电化学腐蚀中,负极反应是________,正极反应是__________。
(2)从铁钉被腐蚀的情况可知引起和促进铁钉被腐蚀的条件是_____________。
(3)为防止铁的锈蚀,工业上普遍采用的方法是___________(答两种方法)。