某小组同学利用下图装置(夹持仪器已省略)制备溴苯,并探究该反应原理。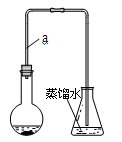
I.制备溴苯
(1)装置中长导管a的作用是 、导出气体。
(2)本实验所获得的溴苯为褐色,是因为 。
II.分离提纯
已知,溴苯与苯互溶,液溴、苯、溴苯的沸点依次为59℃、80℃、156℃。同学们设计了如下流程: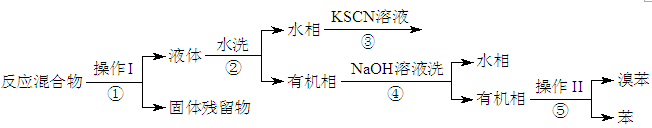
(3)操作Ⅱ为 。
(4)流程②和④中,需要用到的玻璃仪器是烧杯、 ;流程③的现象为 ,流程④的作用是 。
III.探究原理
(5)反应结束后,某同学取少量锥形瓶中的液体于试管中,再滴入几滴AgNO3溶液,出现浅黄色浑浊,从而判断反应一定生成了HBr。你认为该同学的判断 (填“合理”、“不合理”)。
(6)为探究锥形瓶中溶液的离子,请完成下表探究实验方案(限选试剂:镁粉、四氯化碳、氯水、溴水、蒸馏水)
| 实验步骤 |
预期现象 |
结论 |
| 1.将锥形瓶中的液体转入分液漏斗,加足量 ① ,振荡后分液。分别取少量 ② 层溶液于试管A、B中 |
|
|
| 2.向试管A中加入少量 ③ 和四氯化碳,振荡后静置; |
溶液分层,下层显 ④ 色 |
锥形瓶中液体含大量Br- |
| 3.向试管B中加入 ⑤ 。 |
有汽泡生成 |
锥形瓶中液体含大量 ⑥ |
根据上述结论推断,制备溴苯的反应属于 反应,其反应方程式为 。
某学习小组甲利用中和反应原理和DIS系统(即数字化信息系统,由传感器、数据采集器和计算机组成)测定某氨水的物质的量浓度,以测量溶液导电能力来判断滴定终点。请回答:
(1)实验时量取10.00mL氨水样品,配制成100mL待测氨水,则该步操作中需要的仪器有_________________(填仪器名称)。
(2)量取20.00mL上述溶液倒入洁净干燥锥形瓶中,连接好DIS系统。如果锥形瓶中含有少量蒸馏水,是否会影响测量结果_______(填“是”“否”“不能确定”)。
(3)①滴定管盛放盐酸前,要先__________________,用少量蒸馏水洗涤后,再_________________,然后加入盐酸调整液面至凹液面的最低点处于滴定管的_________________。
②向锥形瓶中滴加0.10mol·L-1的盐酸,计算机屏幕上显示出溶液导电能力与加入盐酸体积关系的曲线图。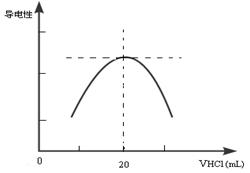
写出氨水与盐酸反应的离子方程式___________________________;该氨水样品的物质的量浓度为_____________。
(4)另一学习小组乙认为上述测量结果仍存在一定误差,因为生成的NH4Cl 是强酸弱碱盐,会发生水解而使NH4+浓度下降,这样,恰好完全反应时NH4+浓度不是最大值,溶液导电性就不是最大值。你认为乙学习小组的结论是否正确?________,理由是___________________。
实验室用下图装置制取少量溴苯,试填写下列空白。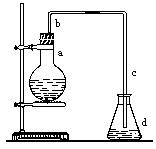
(1)在烧瓶a中装的试剂是、、。
(2)请你推测长直导管b的作用是 。
(3)请你推测导管c的下口可否浸没于液面中
(4)写出烧瓶a中所有反应的方程式(标明条件)并指出有机反应类型________。
某学生为了探究铁与盐酸反应过程中的速率变化,他在100 mL稀盐酸中加入足量的铁粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
 时间(min) 时间(min) |
1 |
2 |
3 |
4 |
5 |
| 氢气体积(mL) |
50 |
120 |
232 |
290 |
310 |
(气体 体积为标准状况下测定的体积)
体积为标准状况下测定的体积)
(1)哪一时间段(指0~1、1~2、2~3、3~4、4~5 min )反应速率最大,
)反应速率最大,
原因是 。
。
(2)哪一段时段的反应速率最小,原因是。
(3)如果反应太激烈,为了减缓反应速率而又不影响产生氢气的量,他在盐酸中分别加入等体积的下列溶液,你认为可行的是(填编号)。
| A.蒸馏水 | B.NaOH溶液 | C.Na2CO3溶液 | D.CuSO4溶液 |
(4)2~3分钟时间段以盐酸的浓度变化来表示的该反应速率为。
某校研究性学习小组用相同大小的铜片和锌片为电极研究水果电池,得到的实验数据如下表所示:(已知果汁是显酸性的)
| 实验编号 |
水果种类 |
电极间距离/㎝ |
电流大小/µA |
| ① |
西红柿 |
1 |
98.7 |
| ② |
西红柿 |
2 |
72.5 |
| ③ |
苹果 |
2 |
27.2 |

(1)该实验的目的是探究水果种类和_______________对水果电池电流大小的影响。
(2)能表明水果种类对电流大小有影响的实验编号是 和 __________。
__________。
(3)上图所示的装置中,负极的电极反应式为 ,正极附近区域的C(H+)将 (填“增大”、“减小”、“不变”),总反应离子方程式为 。
已知氨可以与灼热的氧化铜反应得到氮气和金属铜,反应方程式为2NH3+3CuO  N2+3H2O+3Cu,用示意图中的装置可以实现该反应,A中加的是氯化铵和氢氧化钙固体,C中的固体是氧化铜。回答下列问题:
N2+3H2O+3Cu,用示意图中的装置可以实现该反应,A中加的是氯化铵和氢氧化钙固体,C中的固体是氧化铜。回答下列问题:
(1)A中发生反应的化学方程式是。
检验氨气通常采用的方法是_________,其现象是__________。
(2)B中加入的物质是,其作用是。
(3)实验时C中观察到的现象是 ,该反应中氨的作用是_______(填氧化剂或还原剂)。
,该反应中氨的作用是_______(填氧化剂或还原剂)。
(4)实验时在D中收集到的液态物质是,E中收集到的气体是__________。
(5)若要检验反应生成的水,可将试管D及烧杯部分改成两个相连的干燥管,(一种类似于U型管作用,内装固体干燥剂的管子)第一个干燥管X内装有______,现象是_______;第二个干燥管Y内装有碱石灰,作用是_____________。