在下图转化关系中,固体甲的焰色反应呈黄色,M为常见的液体物质,I为一常见金属,酸G是重要的化工产品和化工原料;固体H能够溶解在A溶液和酸G中,且H为良好的耐火材料(图中部分产物没有列出)。
(1)固体甲与液体M反应的方程式为______。A溶液与固体H反应的离子方程式为______。
(2)固体乙的化学式为_______。液体M的电子式为_______。
(3)反应①~⑦中属于氧化还原反应的为_______(填写反应序号)。
(4)若I与C的稀溶液不反应,只能与G的浓溶液在加热条件下反应,则反应⑦的化学方程式为_______。
(5)若由黄铁矿(FeS2)与气体B反应来生产气体E,且每生成1 mol E放出426.5 kJ的热量,该反应的热化学方程式为_______ 。
(每空2分,共10分)某烃A 0.2 mol 在氧气中完全燃烧后,生成CO2和H2O各1.2 mol。试回答:
(1)烃A的分子式为_____________。
(2)若取一定量的烃A完全燃烧后,生成CO2和H2O各3 mol,则有________g烃A参加了反应,燃烧时消耗标准状况下的氧气___________L。
(3)若烃A不能使溴水褪色,但在一定条件下能与氯气发生取代反应,其一氯取代物只
有一种,则烃A的结构简式为__________________。
(4)若烃A能使溴水褪色,在催化剂作用下,与H2加成,其加成产物经测定分子中含有
4个甲基,烃A可能有的结构简式为______________(写出一种即可)
将煤粉隔绝空气加强热,除主要得到焦炭外,还能得到下表所列的物质:
| 序号 |
① |
② |
③ |
④ |
⑤ |
⑥ |
⑦ |
| 名称 |
甲烷 |
一氧化碳 |
乙烯 |
苯 |
甲苯 |
苯酚 |
氨水 |
(1)表中所列物质不属于有机物的是(填序号):。
(2)能与溴水反应使之褪色的烃是(填序号):。
(3)彼此互为同系物的是(填序号):。
(4)能发生加聚反应、生成物可用作制造食品包装袋的是(填序号),
该物质发生加聚反应的化学方程式为:。
(5)甲苯的一氯取代产物有种。
(8分)请根据反应:Fe + Cu2+ = Fe 2++ Cu 设计原电池:
(1)(2分)画出实验的简易装置图:(用铅笔画图)
(2)(6分)写出电极反应式,正极:,负极:。当反应进行到一段时间后取出电极材料,测得某一电极增重了6.4g,则反应共转移了的电子数是。
(18分)下表是元素周期表的一部分,回答有关问题: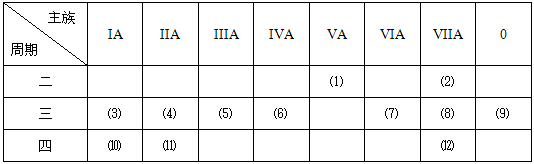
(1)写出下列元素符号:⑴,⑹,⑺,⑾
(2)在这些元素中,最活泼的金属元素是,最活泼的非金属元素是,最不活泼的元素是,(填元素符号)最不活泼的元素的结构示意图是。
(3)在这些元素中的元素的最高价氧化物对应的水化物中,酸性最强的是,碱性最强的是,呈两性的是,(填化学式);
(4)在这些元素中,原子半径最小的是,原子半径最大的是(填名称)
(5)元素(3)可以和氧气反应形成淡黄色固体,写出该物质的电子式:;该物质中存在的化学键有。
(6)用电子式表示由元素(8)和(10)形成化合物的过程:。
在元素周期表中有个周期,个族,其中有个主族,周期序数等于原子的,主族序数等于原子的。同一周期从左到右,金属性逐渐,非金属性逐渐;同一主族从上到下,金属性逐渐,非金属性逐渐.(填“增强”或“减弱” )