铁矿石是工业炼铁的主要原料之一,其主要成分为铁的氧化物(设杂质中不含铁元素和氧元素,且杂质不与硫酸反应)。某研究性学习小组对某铁矿石中铁的氧化物的化学式进行探究。
Ⅰ.铁矿石中含氧量的测定,以下实验过程不完整,请补充完整。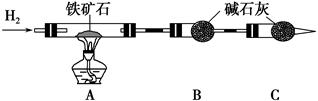
(1)按上图组装仪器,并______________________________________________;
(2)将8.0 g铁矿石放入硬质玻璃管中,装置B、C中的药品如图所示(夹持仪器均省略);
(3)从左端导气管口处不断地缓缓通入H2,____________________________,
点燃A处酒精灯;
(4)充分反应后,撤掉酒精灯,________________________________________;
(5)测得反应后装置B增重2.25 g,则铁矿石中氧的百分含量为________。
Ⅱ.铁矿石中含铁量的测定,流程如下。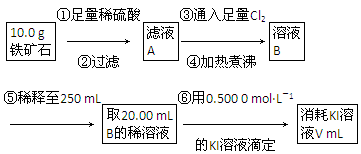
(1)步骤④中煮沸的作用是___________________________________________。
(2)步骤⑤中用到的玻璃仪器有烧杯、胶头滴管、250 mL容量瓶、________。
(3)下列有关步骤⑥的操作中说法正确的是________。
a.因为碘水为黄色,所以滴定过程中不需加指示剂
b.锥形瓶不需要用待测液润洗
c.滴定过程中可利用淀粉溶液作指示剂
d.滴定过程中,眼睛注视滴定管中液面变化
e.滴定结束后,30 s内溶液不恢复原来的颜色,再读数
f.滴定结束后,滴定管尖嘴部分有气泡,则测定结果偏大
(4)若滴定过程中消耗0.500 0 mol·L-1 KI溶液20.00 mL,则铁矿石中铁的百分含量为________。
Ⅲ.由Ⅰ、Ⅱ可以推算出该铁矿石中铁的氧化物的化学式为________。
下下图所示五元环代表A、B、C、D、E五种化合物,圆圈交叉部分指两种化合物含有一种相同元素;五种化合物由四种短周期元素形成,每种化合物仅含有两种元素。A是工业制取硝酸的主要原料之一;B、E分子中所含电子数都为18,B不稳定,具有较强的氧化性,E是由六个原子构成的分子,可作火箭燃料;C是工业制光导纤维的主要原料;D中所含的两种元素的原子个数之比为3∶4。根据以上信息回答下列问题: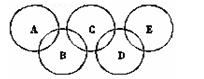
(1)A用于工业制取硝酸所发生反应的化学方程式。
(2)D的化学式是。
(3)B在实验室中可以用于制取某种常见气体,其反应的化学方程式
为。
(4)B与E反应可生成单质G和一种常见的液体H,其反应的化学方程式为
。
(5)用化学方程式表示C的另一种用途。
铁是一种历史悠久、应用最广泛、用量最大的金属。有三位同学分别用铁粉
进行如下探究实验:
(1)甲同学用已部分生锈的废铁屑制作印刷电路板的腐蚀剂,并回收铜。探究过程如下:
①步骤②中,除发生反应Fe+2HClFeCl2+H2↑外,其他可能反应的离子方程式
为:。
②可以验证溶液B中是否含有Fe2+的一种试剂是(填选项序号)
a.稀硫酸 b.铁 c.硫氰化钾 d.酸性高锰酸钾溶液
(2)乙同学欲用少量Fe粉与足量浓硫酸反应得到硫酸亚铁。有人认为不论常温还是加热的条件下均不可行,理由是
于是乙同学将上述方案做如下改进后可获得FeSO4·7H2O,请填写下列括号中的空白: (3)丙同学为测试一铁片中铁元素的含量,在实验室中用m g铁片完全溶解于过量稀硫酸中,准确测定出反应生成氢气的体积为V mL (已折算成标准状况),则该铁片中铁的质量分数为(用含m、V的代数式表示) 。若排除实验仪器和操作的影响因素,试对上述方案测定结果的准确性做出判断和分析:方案 (填“准确”“不准确”“不一定准确”),理由是
(3)丙同学为测试一铁片中铁元素的含量,在实验室中用m g铁片完全溶解于过量稀硫酸中,准确测定出反应生成氢气的体积为V mL (已折算成标准状况),则该铁片中铁的质量分数为(用含m、V的代数式表示) 。若排除实验仪器和操作的影响因素,试对上述方案测定结果的准确性做出判断和分析:方案 (填“准确”“不准确”“不一定准确”),理由是
.
实验室需要0.80 mol/L NaOH溶液475 mL和0.40 mol/L硫酸溶液500 mL。根据这两种溶液的配制情况回答下列问题: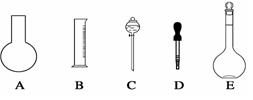
(1)如图所示的仪器中配制溶液肯定不需要的是(填序号),配制上述溶液还需用到的玻璃仪器是(填仪器名称)。
(2)根据计算用托盘天平称取NaOH的质量为g。在实验中其他操作均正确,若定容时俯视视刻度线,则所得溶液浓度0.8 mol/L(填“大于”、“等于”或“小于”,下同)。若定容时,有少许蒸馏水洒落在容量瓶外,则所得溶液浓度0.8 mol/L。
(3)根据计算得知,所需质量分数为98%、密度为1.84 g/cm3的浓硫酸的体积为mL
某校化学研究性学习小组在学习了金属的知识后,探究Cu的常见化合物性质。过程如下:
提出猜想
① 在周期表中,Cu、Al位置接近。Cu不如Al活泼,Al(OH)3具有两性,Cu(OH)2也具有两性吗?
② 常况下,+2价Fe的稳定性小于+3价Fe,+1价Cu的稳定性也小于+2价Cu吗?
③ CuO有氧化性,能被H2、CO等还原,也能被氮的气态氢化物还原吗?
实验探究
⑴ 解决问题①需用到的药品有CuSO4溶液、(填试剂),同时进行相关实验。
⑵ 解决问题②的实验步骤和现象如下:取一定量的Cu(OH)2固体,加热至80 ℃~100 ℃时,得到黑色固体粉末,继续加热到1000 ℃以上,黑色粉末全部变成红色粉末氧化亚铜。向氧化亚铜中加入过量稀硫酸,得到蓝色溶液,同时观察到容器中还有红色固体存在。根据以上现象写出氧化亚铜和稀硫酸反应的离子方程式。
⑶为解决问题③,设计了如下的实验装置(夹持装置未画出):
在实验中观察到CuO变成红色物质,无水CuSO4变成蓝色,生成物中还有一种无污染的单质气体Y。现有氮的某种气态氢化物X气体0. 0l mol,缓缓通过红热的氧化铜玻璃管完全反应后,测得C装置增重0. 36g并收集到单质气体Y0.28g。
X气体的摩尔质量,B中发生反应的化学方程式为。
(4)请猜测用上述装置测量时有可能产生误差的原因
.(答1条即可)
实验结论
⑴Cu(OH)2具有两性。证明Cu(OH)2具有两性的实验现象是
.。
⑵ 根据实验方案⑵,得出的+1价Cu和+2价Cu稳定性大小的结论是:
.
⑶ CuO能够被氮的气态氢化物还原。
某校化学研究性学习小组在学习了金属的知识后,探究Cu的常见化合物性质。过程如下:
提出猜想
① 在周期表中,Cu、Al位置接近。Cu不如Al活泼,Al(OH)3具有两性,Cu(OH)2也具有两性吗?
② 常况下,+2价Fe的稳定性小于+3价Fe,+1价Cu的稳定性也小于+2价Cu吗?
③ CuO有氧化性,能被H2、CO等还原,也能被氮的气态氢化物还原吗?
实验探究
⑴ 解决问题①需用到的药品有CuSO4溶液、(填试剂),同时进行相关实验。
⑵ 解决问题②的实验步骤和现象如下:取一定量的Cu(OH)2固体,加热至80 ℃~100 ℃时,得到黑色固体粉末,继续加热到1000 ℃以上,黑色粉末全部变成红色粉末氧化亚铜。向氧化亚铜中加入过量稀硫酸,得到蓝色溶液,同时观察到容器中还有红色固体存在。根据以上现象写出氧化亚铜和稀硫酸反应的离子方程式。
⑶为解决问题③,设计了如下的实验装置(夹持装置未画出):
在实验中观察到CuO变成红色物质,无水CuSO4变成蓝色,生成物中还有一种无污染的单质气体Y。现有氮的某种气态氢化物X气体0. 0l mol,缓缓通过红热的氧化铜玻璃管完全反应后,测得C装置增重0. 36g并收集到单质气体Y0.28g。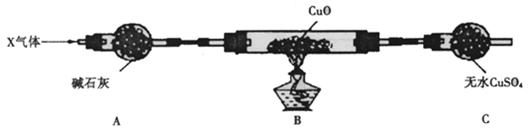
X气体的摩尔质量,B中发生反应的化学方程式为。
(4)请猜测用上述装置测量时有可能产生误差的原因
.(答1条即可)
实验结论
⑴Cu(OH)2具有两性。证明Cu(OH)2具有两性的实验现象是
.。
⑵ 根据实验方案⑵,得出的+1价Cu和+2价Cu稳定性大小的结论是:
.
⑶ CuO能够被氮的气态氢化物还原。