脱水环化是合成生物碱类天然产物的重要步骤,某生物碱合成路线如图: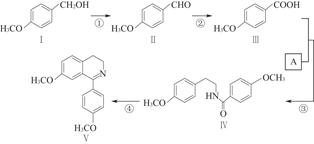
(1)化合物Ⅱ的化学式为 。
(2)反应①的化学方程式为(不要求写出反应条件) 。
(3)化合物A的结构简式为 。
(4)下列说法正确的是 。
| A.化合物Ⅱ能发生银镜反应 |
| B.化合物Ⅰ~Ⅴ均属于芳香烃 |
| C.反应③属于酯化反应 |
| D.化合物Ⅱ能与4 mol H2发生加成反应 |
E.化合物Ⅰ、Ⅱ、Ⅲ均能与金属钠反应放出氢气
(5)化合物Ⅵ与化合物Ⅲ互为同分异构体,Ⅵ中含有酯基,且能与FeCl3溶液发生显色反应,其苯环上的一氯代物只有2种。写出一种满足上述条件的Ⅵ的结构简式: 。
(6)化合物Ⅶ(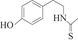 )在一定条件下也能发生类似上述第④步骤的环化反应,化合物Ⅶ环化反应产物的结构简式为 。
)在一定条件下也能发生类似上述第④步骤的环化反应,化合物Ⅶ环化反应产物的结构简式为 。
《化学与生活》
(1)人体健康与食品等关系密切。
①生活中应合理地摄取人体必需的元素,体内________ 含量过高,会引起甲状腺疾病[
②。糖类、油脂、蛋白质都是人体必需的营养物质。其中蛋白质被摄入人体后,在酶的作用下最终水解为_______________________(写名称)。
③棉花纤维的化学成分是(写化学式)。
(2)中国是世界上最早研究和生产合金的国家之一。
①在原子反应堆中得以广泛应用的钠钾合金在常温下呈液态,说明合金的熔点比其成分金属的熔点。
②黄铜(铜锌合金)外观和金(Au)相似,常被误认为黄金。
试写出一种鉴别黄铜与黄金的化学方法。铜器表面容易生成一层薄薄的铜绿[主要成份是Cu2(OH)2CO3],请写出铜在潮湿的空气发生电化学腐蚀时的负极反应式;用盐酸可以除去铜器表面的铜绿,该反应的化 学方程式为。
学方程式为。
③下列对金属制品采取的防护方法不正确的是(填序号)。
A.在电线的外面包上一层塑料层
B.在自行车钢圈上镀上一层金属铬
C.在海轮的铁制外壳上焊上铜块
(3)生活处处有化学,化学与生产、生活密切相关。
①小孩误服重金属盐后,应立即,以减少人体蛋白质中毒的程度。
②食品添加剂亚硝酸钠的外观像食盐,并有咸味,但亚硝酸钠有很强的毒性。亚硝酸钠属于(选填“调味剂”、“防腐剂”或“着色剂”)。
③维生素C的结构为


 它是一种水溶性的维生素,缺乏VC会使人患上病。切取一片新鲜水果,向切面上滴加淀粉溶液和碘水,若出现,说明新鲜水果中含有VC,这是利用VC具有(填
它是一种水溶性的维生素,缺乏VC会使人患上病。切取一片新鲜水果,向切面上滴加淀粉溶液和碘水,若出现,说明新鲜水果中含有VC,这是利用VC具有(填 “氧化”或“还原”)性质。
“氧化”或“还原”)性质。
④乙酰水杨酸( )的俗名为阿司匹林,是常用药。它遇水能缓慢地水解生成水杨酸,则水杨酸的结构简式可表示为
)的俗名为阿司匹林,是常用药。它遇水能缓慢地水解生成水杨酸,则水杨酸的结构简式可表示为 。
。
核能源已日益成为当今世界的主要能源。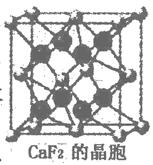
(1)核能原料UO2可通过三碳酸铀酰铵(NH4)4[UO2 (CO3)3]直接煅烧还原制得。UO2晶体属CaF2型面心立方结构(CaF2的晶胞示意图如图),则UO2晶体U4+的配位数为;
 |
三碳酸铀酰铵中含有化学键类型有;
A.离子键 B.σ键 C.π键 D.氢键 E.配位键
根据价层电子对互斥理论推测CO32-的空间构型为;写出一种与CO32-互为等电子体且属于非极性分子的微粒的化学式。
(2)为了获得高浓度的235U,科学家们采用“气体扩散法”:到目前为止,UF6是唯一合适的化合物。UF6在常温常压下是固体,在56.4℃即升华成气体。UF6属于晶体。’
(3)放射性碘是重要的核裂变产物之一,因此放射性碘可以作为核爆炸或核反应堆泄漏事故的信号核素 。写出131I基态原子的价电子排布式。
。写出131I基态原子的价电子排布式。
下表列出了前20号元素中的某些元素性质的有关数据:
| 元素编号 元素性质 |
① |
② |
③ |
④ |
⑤ |
⑥ |
⑦ |
⑧ |
⑨ |
⑩ |
| 原子半径(10-10m) |
1.52 |
2.27 |
0.74 |
1.43 |
0.77 |
1.10 |
0.99 |
1.86 |
0.75 |
0.71 |
| 最高价态 |
+1 |
+1 |
/ |
+3 |
+4 |
+5 |
+7 |
+1 |
+5 |
/ |
| 最低价态 |
/ |
/ |
-2 |
/ |
-4 |
-3 |
-1 |
/ |
-3 |
-1 |
试回答下列问题:
(1)以上10种元素的原子中,失去核外第一个电子所需能量最少的是(填写编号)。
(2)上述⑤、⑥、⑦三种元素中的某两种元素形成的化合物中,每个原子都满足最外层为8电子稳定结构的物质可能是(写分子式)。某元素R的原子半径为1. 02×10-10m,该元素在周期表中位于;若物质Na2R3是一种含有非极性共价键的离子化合物,请你写出该化合物的电子式。
02×10-10m,该元素在周期表中位于;若物质Na2R3是一种含有非极性共价键的离子化合物,请你写出该化合物的电子式。
(3)元素⑤的某种单质具有平面层状结构,同一层中的原子构成许许多多的正六边形,此单质与熔融的②单质相互作用,形成某种青铜色的物质(其中的元素②用“●”表示),原子分布如图所示,该物质的化学式为。
水是生命之源,它与我们的生活密切相关。在化学实验和科学研究中,水也是一种常用的试剂。
(1)水分子中氧原子在基态时核外电子排布式为__________;
(2)下列是钠、碘、金刚石、干冰、氯化钠晶体的晶胞图(未按顺序排序)。与冰的晶体类型相同的是_____(请用相应的编号填写)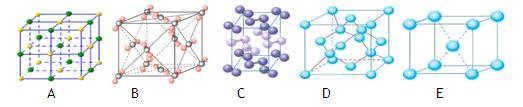
(3)在冰晶体中,每个水分子与相邻的4个水分子形成氢键(如图所示),已知冰的升华热是a kJ/mol,除氢键外,水分子间还存在范德华力(b kJ/mol),则冰晶体中氢键的“键能”是_________kJ/mol;
(4)将白色的无水CuSO4溶解于水中,溶液呈蓝色,是因为生成了一种呈蓝色的配合离子。请写出生成此配合离子的离子方程式: 。
。
(1)由A、B两元素组成的离子晶体结构(甲)如图所示,则该晶体的化学式是:。
(2)C原子的最外层电子排布为nsnnpm,其某一激发态可使这两个亚层的每一个轨道都处于充满状态,1个C原子与2个D原子结合,使双方都达 到8电子稳定结构。则在C与D形成的分子中,C原子发生轨道的杂化方式是
到8电子稳定结构。则在C与D形成的分子中,C原子发生轨道的杂化方式是 ,分子构型是,从成键方式
,分子构型是,从成键方式 看,该分子中含有的共价键的类型和数目分别是。
看,该分子中含有的共价键的类型和数目分别是。
(3)C与D形成的常见晶体(乙),与甲晶体的熔点相比,乙甲,其原因是。