下面是元素周期表的一部分,参照元素①-⑧在表中的位置,请用化学用语回答下列问题:
| 族 周期 |
IA |
|
0 |
|||||
| 1 |
① |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
|
| 2 |
|
|
|
② |
③ |
④ |
|
|
| 3 |
⑤ |
|
⑥ |
⑦ |
|
|
⑧ |
|
(1)④、⑤、⑥的原子半径由大到小的顺序为(元素符号)________________________。
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是(填化学式)________ 。
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的化学式:_______________。
(4)由②和④组成的化合物与⑤的同周期相邻主族元素的单质反应的化学方程式为:_______。
(5)⑥单质与⑤的最高价氧化物的水化物反应的离子方程式为 。
(6)若用①②组成最简单的有机物作为燃料电池的原料,请写出在碱性介质中燃料电池负极的电极反应式: 。
(7)燃煤废气中的含有氮氧化物(NOx)、二氧化碳等气体,常用下列方法对燃煤废气进行脱硝处理时,常利用甲烷催化还原氮氧化物。
如:CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) , △H=-574 kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) , △H=-1160 kJ·mol-1
则CH4(g)将NO2(g)还原为N2(g)等的热化学方程式为 。
硝酸是一种重要的化工原料,工业上通常采用氨氧化法制取。某校化学兴趣小组的同学以氯化铵和氢氧化钙为主要原料并设计了下列装置来制硝酸(三氧化二铬为催化剂,加热及夹持装置未画出):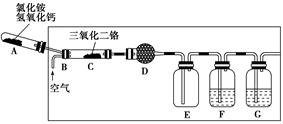
回答下列问题:
(1)实验时,A、C两装置均需加热,应先加热________装置,原因是
________________________________________________________________________。
(2)D装置中应填充的物质是________,该物质的主要作用是____________________。
(3)E装置的作用是__________________,F、G装置中的物质分别是________、________。
(4)若保留上图中黑色粗线框内的装置但去掉通空气的导管B,将C装置中的双孔橡皮塞换成单孔橡皮塞,请你用图示的方法设计一个最简单的实验方案同样完成硝酸的制取(在下面的方框中画出装置图并注明所用药品的名称)。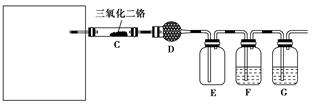
可用如图所示装置制取少量乙酸乙酯(酒精灯等在图中均已略去)。请填空: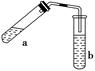
(1)试管a中需要加入浓硫酸、冰醋酸和乙醇各2 mL,正确的加入顺序及操作是
________________________________________________________________。
(2)为防止a中的液体在实验时发生暴沸,在加热前应采取的措施是
________________________________________________________________________。
(3)实验中加热试管a的目的是:①__________________;②____________________。
(4)试管b中加有饱和Na2CO3溶液,其作用是
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
(5)反应结束后,振荡试管b,静置,观察到的现象是
________________________________________________________________________。
某课外小组设计制备乙酸乙酯的装置如图所示。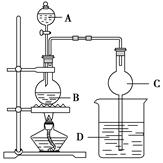
查阅资料得到:
Ⅰ.CaCl2可与乙醇生成难溶于水的混合物CaCl2·2C2H5OH;
Ⅱ.数据:
| 物质 |
乙醇 |
乙酸 |
乙酸乙酯 |
浓硫酸(98%) |
| 沸点/℃ |
78.5 |
117.9 |
77.1 |
338.0 |
实验主要步骤如下:
①按图连接好装置(装置气密性良好),A中盛有浓硫酸,B中盛有乙醇和乙酸钠的混合溶液、碎瓷片,D中盛有含酚酞的饱和Na2CO3溶液。
②用小火均匀加热有混合溶液的烧瓶5~10 min。
③待D收集到一定量产物后停止加热,撤出C,将D混合物搅拌,然后静置待分层。
请根据设计要求帮助解决下列问题:
(1)浓硫酸的作用是
________________________________________________________________________。
(2)实验中饱和碳酸钠溶液的作用是(填字母):________。
A.中和乙酸和乙醇
B.中和乙酸并吸收部分乙醇
C.乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中更小,有利于分层析出
D.加速酯的生成,提高其产率
(3)该小组将教材实验装置图4-2-3(a)进行了改进,一是反应器大试管换成了烧瓶,其优点是________________;二是在导管中添加了球形干燥管,优点是
________________________________________________________________________
________________________________________________________________________。
步骤②中需要小火均匀加热操作,其主要理由是:
________________________________________________________________________
________________________________________________________________________。
在化学实验中同一套实验装置可以用于不同的实验。下图所示装置可以完成以下实验: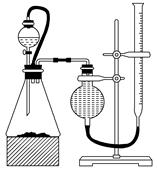
| A.锌片纯度的测定; |
| B.醇中羟基数的测定; |
| C.盐酸的物质的量浓度的测定; |
| D.NaOH溶液的物质的量浓度的测定。 |
现在在标准状况下进行实验。可供选择的试剂有Na、Al、Zn(含杂质)、分子式为C2H6O2的有机物、水、未知浓度的盐酸、未知浓度的NaOH溶液等。
(1)这四个实验中需要共同测定的量是
________________________________________________________________________;
(2)测定过程中,根据测定目的的不同,反应物的用量很重要,而且是实验成败的关键之一,比如实验A中盐酸要过量,实验B中________要过量,实验D中________要过量;
(3)已知在B实验中消耗m g分子式为C2H6O2的有机物,在标准状况下测得气体的体积为V mL,则该有机物中的羟基数为________,若一个该有机物分子中羟基数为2,则其结构简式为________;
(4)请写出D实验所涉及的离子方程式
________________________________________________________________________
________________________________________________________________________;
(5)装置的气密性很重要,请你说明该装置的气密性的检查方法
________________________________________________________________________
________________________________________________________________________。
为了探究乙醇和金属钠反应的原理,做了如下四个实验:
实验一:向小烧杯中加入无水乙醇,再放入一小块金属钠,观察现象,并收集产生的气体。
实验二:设法检验实验一收集到的气体。
实验三:向试管中加入3 mL水,并加入一小块金属钠,观察现象。
实验四:向试管中加入3 mL 乙醚(结构简式为C2H5—O—C2H5),并加入一小块金属钠,观察现象。
回答以下问题:
(1)简述实验二中检验气体的实验方法及作出判断的依据:
________________________________________________________________________
________________________________________________________________________。
(2)从结构上分析,该实验选取水和乙醚做参照物的原因是
________________________________________________________________________
________________________________________________________________________。
(3)实验三的目的是欲证明
________________________________________________________________________;
实验四的目的是欲证明
________________________________________________________________________;
根据实验三和实验四的结果,可以证明乙醇和金属钠反应的化学方程式应为________________________________________________________________________。