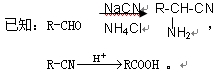
氯吡格雷(clopidogrel)是一种用于抑制血小板聚集的药物。以A(C7H5OCl)为原料合成氯吡格雷的路线如下:
完成下列填空:
(1)C中含氧官能团的名称为 ,C→D的反应类型是 。
(2)Y的结构简式为 ,在一定条件下Y与BrCl(一氯化溴,与卤素单质性质相似)按物质的量1:1发生加成反应,生成的产物可能有 种。
(3)C可在一定条件下反应生成一种产物,该产物分子中含有3个六元环。该反应的化学
程式为 。
(4)由E转化为氯吡格雷时,生成的另一种产物的结构简式为 。
(5)写出A(芳香族化合物)的所有同分异构体的结构简式(包括A本身) 。
(6)
写出由乙烯、甲醇为有机原料制备化合物 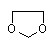 的合成路线流程图(无机试剂任选)。合成路线流程图示例如下:
的合成路线流程图(无机试剂任选)。合成路线流程图示例如下:
CH3CH2OH 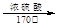 CH2=CH2
CH2=CH2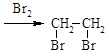
。
[化学—选修5:有机化学基础]
G是一种医药中间体,常用来制备抗凝血药,可通过下列路线合成:
(1)化合物G的分子式为。B转化为C的反应所属反应类型为。
(2)化合物D的名称为,它的核磁共振氢谱应有组不同类型的峰,它与碳酸氢钠溶液反应的化学方程式为。
(3)化合物E的同分异构体中,能够使三氯化铁溶液显紫色,且能 够水解生成化合物B的有种。这其中核磁共振氢谱图有四组不同类型峰的同分异构体的结构简式为。
够水解生成化合物B的有种。这其中核磁共振氢谱图有四组不同类型峰的同分异构体的结构简式为。
(4)请分别写出A→B、D→E两个转化过程中的反应方程式:、。
【化学——选修3:物质结构与性质】
在A、B、C三种元素中,A元素原子的价电子排布为2s22p5,B元素K、L能层上的电子数与M、N层上的电子数相同。C元素的原子序数等于A、B两元素原子序数之和,C的单质在生产生活中具有许多用途,它可在硫酸铜溶液中用电解法进行精炼。请回答以下问题:
(1)已知C元素的电负性数值为1.9,则A、C两元素的原子之间应形成键(填“共价”或“离子”);
(2)C元素的价电子排布式为____;
(3)在A元素氢化物的水溶液中,存在有种不同类型的氢键;
(4)SO42—中S原子的杂化轨道类型是____,SO42—的立体构型是____;
(5)一种铜金合金晶体具有面心立方最密堆积的结构,在晶胞中Cu原子处于面心,Au原子处于顶点位置,则该合金中Cu原子与Au原子数量之比为_______;该晶体中,原子之间的作用力是________;
(6)在A、B两元素所形成晶体的晶胞中,位于六面体顶点 和面心上的元素为(填具体的元素符号)。
和面心上的元素为(填具体的元素符号)。
【化学——选修2:化学与技术】
水是一种重要的自然资源,是人类赖以生存不可缺少的物质。水质优劣直接影响人体健康。请回答下列问题:
(1)天然水中溶解的气体主要有、。
(2)天然水在净化处理过程中加入的混凝剂可以是,其净水作用的原理是。
(3)水的净化和软化的区别是。
(4)硬度为1°的水是指每升水含10mgCaO或与之相当的物质(如7.1mgMgO)。若某天然水中c(Ca2+)=1.2×10—3mol/L,c(Mg2+)=6×10—4mol/L,则此水的硬度为。
(5)若(4)中的天然水还含有c(HCO3—)=8×10—4mol/L,现要软化10m3这种天然水,则需先加入Ca(OH)2g,后加入Na2CO3g。
化合物A俗称石灰氮,以前是一种常用的肥料,其含氮量可高达 35.0%,钙含量为50%。它可以用CaCO3通过下列步骤方便地制出:
(1)已知固态二元化合物D中钙含量为62.5%,则D的化学式为。
(2)请推算出A的化学式。。
(3)分别写出上述过程中生成D和A的化学方程式。 ;。
(4) 将A放入水中,会重新生成CaCO3并放出刺激性气味的气体,请写出发生反应的化学方程式。。
(5)已知CaCO3与CaSO4的溶度积分别为2.8×10—9、9.1×10—6。由此可知二者的溶解度的大小关系为CaCO3CaSO4。在锅炉除垢操作中,要先用碳酸钠溶液将水垢中的硫酸钙转化成为碳酸钙。其主要原因是 。
。
炼锌厂产生的工业废渣——锌渣(除了含Zn外,还含有Fe、Al、Cd和SiO2等杂质),利用锌渣制取并回收ZnSO4·7H2O和金属镉是一个有益的尝试,其流程如下: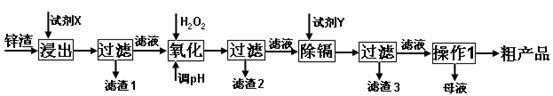
已知:Fe3+、Al3+、Zn2+、Cd2+、Fe2+以氢氧化物完全沉淀时的pH分别为:3.2,4.7,6.5,9.4,9.7;锌的金属活动性比镉强。
试回答下列问题:
(1)“浸出”时用到的“试剂X”为(填名称)。
(2)写出“氧化”过程的离子方程式。
(3)“调pH”过程可以选用。(从以下选项选择, 填序号)
A.H2SO4 B.ZnO C.NaOH
“滤渣2”的主要成分是(填化学式,下同)。
(4)“试剂Y”是______________;“滤渣3”的成分为______________________。
(5)“操作1”的方法是___ ____;在“操作1”时,必须采取的实验措施是。