硫-碘循环分解水制氢主要涉及下列反应:
Ⅰ.SO2+2H2O+I2=H2SO4+2HI
Ⅱ.2HI H2↑+I2
H2↑+I2
Ⅲ.2H2SO4=2SO2+O2↑+2H2O
(1)分析上述反应,下列判断正确的是 。
a.反应Ⅲ易在常温下进行
b.反应Ⅰ中SO2氧化性比HI强
c.循环过程中需补充H2O
d.循环过程中产生1 mol O2的同时产生1 mol H2
(2)一定温度下,向1 L密闭容器中加入1 mol HI(g),发生反应Ⅱ,H2的物质的量随时间的变化如图所示。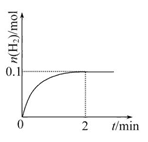
①0~2 min内的平均反应速率v(HI)= 。
②相同温度下,若开始加入HI(g)的物质的量是原来的2倍,则 是原来的2倍。
a.HI的平衡浓度
b.达到平衡的时间
c.平衡时H2的体积分数
(3)实验室用Zn和稀硫酸制取H2,若加入少量下列固体试剂中的 ,产生H2的速率将增大。
a.NaNO3 b.CuSO4 c.Na2SO4 d.NaHSO3
下面是一个四肽,它可以看作是4个氨基酸缩合掉3个分子水而得。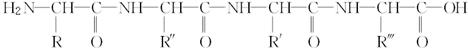
式中,R,R′,R″,R可能是相同的或不同的烃基,或有取代基的烃基;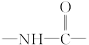 称为肽键。今有一个“多肽”,其分子式是C55H70O19N10,已知将它彻底水解后只得到下列四种氨基酸:
称为肽键。今有一个“多肽”,其分子式是C55H70O19N10,已知将它彻底水解后只得到下列四种氨基酸: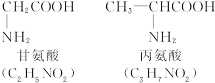
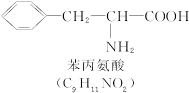
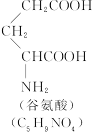
(1)这个“多肽”是___________肽。
(2)该1 mol多肽水解后,有___________mol谷氨酸。
(3)该1 mol多肽水解后,有___________mol苯丙氨酸。
有一新型抗癌药,其分子式为C47H51NO14,它是由如下的酸A和醇反应而生成的一种酯。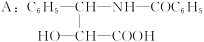
B.R—OH(R是一个含C、H、O的基团)
(1)A在无机酸催化下可水解,其反应方程式为______________________________。
(2)A水解所得到的产物是否是天然蛋白质水解产物?__________,原因是______________。
(3)写出ROH的分子式__________。
α-氨基酸能被HNO2氧化成α-羟基酸,如:
+N2↑+H2O。若丙氨酸可发生如下反应,分别生成A、B、C、D、E五种有机物。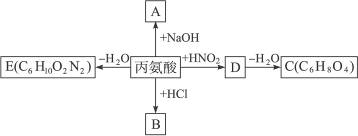
则这些反应产物的结构简式分别为:
A__________;B__________;C__________;D__________;E__________。
氨基乙酸在水溶液中存在如下平衡:
 ,若向氨基乙酸溶液中加入盐酸,则平衡向_________方向移动,有机化合物(写结构简式) _________的浓度增大;若向氨基乙酸溶液中加入NaOH,则平衡向_________方向移动,有机化合物_________的浓度增大。
,若向氨基乙酸溶液中加入盐酸,则平衡向_________方向移动,有机化合物(写结构简式) _________的浓度增大;若向氨基乙酸溶液中加入NaOH,则平衡向_________方向移动,有机化合物_________的浓度增大。
科学家发现某药物M能治疗心血管疾病是因为它在人体内能释放出一种“信使分子”D,并阐明了D在人体内的作用原理。为此他们荣获了1998年诺贝尔生理学或医学奖。
请完成下列问题:
(1)已知M的相对分子质量为227,由C、H、O、N四种元素组成,C、H、N的质量分数依次为15.86%、2.20%和18.50%。则M的分子式是_______________。D是双原子分子,相对分子质量为30,则D的分子式为______________。
(2)油脂A经下列途径可得到M。
图中②的提示:
C2H5OH+HO—NO2 C2H5O—NO2+H2O
C2H5O—NO2+H2O
硝酸硝酸乙酯
反应①的化学方程式是___________________________________________________________。
反应②的化学方程式是___________________________________________________________。
(3)C是B和乙酸在一定条件下反应生成的化合物,相对分子质量为134,写出C所有可能的结构简式。____________________________________
(4)若0.1 mol B与足量的金属钠反应,则需消耗________g金属钠。