下列物质的检验,其结论一定正确的是( )
| A.某溶液中加入BaCl2溶液,产生白色沉淀,加入HNO3后,沉淀不溶解,则该溶液中一定含有SO42- |
| B.某溶液中加入盐酸能产生使澄清石灰水变浑浊的气体,则该溶液中至少有SO32-和CO32-中的一种 |
| C.取少量Na2SO3样品于试管中加水溶解后加入盐酸有气体产生,再加入BaCl2溶液有白色沉淀产生,说明Na2SO3样品已部分被氧化 |
| D.能使湿润的淀粉碘化钾试纸变蓝的一定是Cl2 |
下列物质中,不属于化石燃料的是()
| A.石油 | B.天然气 | C.水煤气 | D.煤 |
已知化学反应2C(s)+O2(g)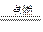 2CO(g)、2CO(g)+O2(g)
2CO(g)、2CO(g)+O2(g)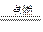 2CO2(g)都是放热反应。据此判断,下列说法中不正确的是(其他条件相同)()
2CO2(g)都是放热反应。据此判断,下列说法中不正确的是(其他条件相同)()
| A.12 g C所具有的能量一定高于28 g CO所具有的能量 |
| B.56 g CO和32g O2所具有的总能量大于88 g CO2所具有的总能量 |
| C.12 g C和32 g O2所具有的总能量大于44 g CO2所具有的总能量 |
| D.将一定质量的C燃烧,生成CO2比生成CO时放出的热量多 |
在相同条件下,一定量的氢气在氧气中充分燃烧并放出热量。若生成液态水放出的热量为Q1;若生成气态水放出的热量为Q2。那么Q1与Q2之间的大小关系是()
| A.Q1>Q2 | B.Q1<Q2 |
| C.Q1=Q2 | D.不能确定 |
已知热化学方程式2H2(g)+O2(g)====2H2O(l)ΔH1="-571.6" kJ·mol-1,则关于化学方程式2H2O(l)====2H2(g)+O2(g) ΔH2的说法中正确的是()
| A.方程式中化学计量数表示分子数 |
| B.该反应ΔH2大于零 |
| C.该反应ΔH2="-571.6" kJ·mol-1 |
| D.该反应可表示36 g水分解时的热效应 |
下列关于反应能量的说法正确的是()
| A.Zn(s)+CuSO4(aq)====ZnSO4(aq)+Cu(s) ΔH="-216" kJ·mol-1,E反应物<E生成物 |
| B.CaCO3(s)====CaO(s)+CO2(g) ΔH="+178.5" kJ·mol-1, E生成物>E反应物 |
C.HI(g)====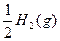 + +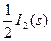 ΔH="-26.5" kJ·mol-1,1 mol HI在密闭容器中分解达平衡时放出26.5 kJ的能量 |
| D.H+(aq)+OH-====(aq)H2O(l) ΔH="-57.3" kJ·mol-1,1 L 1 mol·L-1的NaOH溶液与含0.5 mol H2SO4的浓硫酸混合后放热57.3 kJ |