下列关于各实验装置的叙述中,不正确的是( )
| A.装置①可用于分离C2H5OH和H2O的混合物 |
| B.装置②可用于收集H2、NH3、CO2、Cl2、HCl、NO2等气体 |
| C.装置③中X若为CCl4,可用于吸收NH3或HCl,并防止倒吸 |
| D.装置④可用于干燥、收集NH3,并吸收多余的NH3 |
研究表明生命起源于火山爆发,是因为火山爆发产生的气体中含有1%的羰基硫(COS),已知羰基硫分子中所有原子均满足八电子结构,结合周期表知识,有关说法不正确的是
| A.羰基硫分子为非极性分子 | B.羰基硫的电子式为: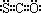 |
| C.羰基硫沸点比CO2高 | D.羰基硫分子中三个原子处于同一直线上 |
法国里昂的科学家发现一种只由四个中子构成的粒子,这种粒子称为“四中子”,也有人称之为“零号元素”。下列有关“四中子”粒子的说法不正确的是
| A.该粒子不显电性 | B.该粒子质量数为4 |
| C.在周期表中与氢元素占同一位置 | D.该粒子质量比氢原子大 |
对于复分解反应:X+Y®Z+W,下列叙述正确的是
| A.若Z是强酸,则X和Y必有一种是强酸 |
| B.若X是强酸,Y是盐,反应后可能有强酸或弱酸生成 |
| C.若Y是强碱,X是盐,则Z或W必有一种是弱碱 |
| D.若W是弱碱,Z是盐,则X和Y必有一种是强碱 |
有下列四组物质,每组物质中均有一种与其他物质所属类别不同。(1)食醋、牛奶、加碘盐、水(2)冰、干冰、氧化铁、金刚石(3)氯化钠、硫酸铜、盐酸、硝酸铝(4)纯碱、烧碱、碳酸钙、氯化亚铁。则各组中的一种物质依次为:
| A.牛奶、干冰、硝酸铝、碳酸钙 | B.水、金刚石、盐酸、烧碱 |
| C.食醋、氧化铁、硫酸铜、氯化亚铁 | D.加碘盐、冰、氯化钠、纯碱 |
下列说法中错误的是
| A.磺化、硝化、风化、钝化都是化学变化 |
| B.蒸馏、干馏、常压分馏、减压分馏、都是物理变化 |
| C.甘油不是油,纯碱不是碱,酚醛树脂不是酯,干冰不是冰 |
| D.水煤气、裂解气、焦炉气、天然气都是混合物 |