某固体混合物含NH4I、NaHCO3、AlCl3、MgBr2、FeCl2中的几种,为确定该固体混合物的成分及各组成成分的物质的量之比,现进行如下实验。
实验Ⅰ:
(1)无色气体为 。
(2)该固体混合物的成分为 。
实验Ⅱ:取一定量的该固体混合物溶于水配成1 L溶液,并向该混合溶液中通入一定量的Cl2,测得溶液中几种阴离子(分别用A-、B-、C-表示)的物质的量与通入Cl2体积的关系如表所示。
| Cl2的体积 (标准状况下)/L |
2.8 |
5.6 |
11.2 |
| n(A-)/mol |
1.25 |
1.5 |
2 |
| n(B-)/mol |
1.5 |
1.4 |
0.9 |
| n(C-)/mol |
a |
0 |
0 |
(3)a= 。
(4)原固体混合物中各组成成分的物质的量之比为 。
(8分)在有机物分子中,常把连有4个不同原子或原子团的碳原子称为“手性碳原子”。含有手性碳原子的分子一般都具有某些光学活性。经测定某新合成物A具有光学活性,其结构简式为:CH3COOCH2CH(CH2OH)CHO。若要在保持A分子中碳原子数不变的前提下,通过适当的反应使A失去光学活性,有两种方法:
(1)有机反应类型:__________反应,对应有机物的结构简式_______________;
(2)有机反应类型:__________反应,对应有机物的结构简式_______________。
氯化银、氢氧化银都能和氨水反应生成Ag(NH3)2+,Ag(NH3)2+能和H+反应:
Ag(NH3)2+ + 2H+=Ag+ +2NH4+,今有一白色固体可能是由Al2(SO4)3、AgNO3、BaCl2、NH4Cl、KOH、Na2S中的两种或三种组成,为了确定该白色固体的成分,进行以下实验:
(1)取白色固体少许,加入适量蒸馏水,充分振荡得无色溶液;
(2)取(1)得到的溶液少许,滴加适量的硝酸,有白色沉淀生成。
由此白色固体必须含有的物质可能有两种组合:
第一种是NH4Cl、_______________________。第二种是_______________________。
在第一种情况下加入足量的稀硝酸时仍有白色沉淀,该白色沉淀是____________。
在第二种情况下加入稀硝酸时也产生白色沉淀,其离子方程式为_______________。
A、B、D均为常见化合物,它们都由两种元素组成,C代表一类化合物;甲、乙、丙都是非金属单质。在一定条件下它们有如下转化关系: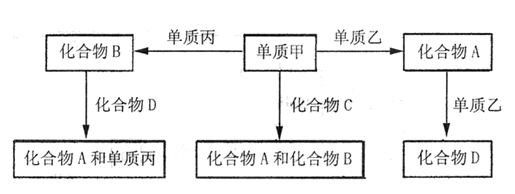
试回答:
(1)单质乙、丙分别为、。
(2)化合物A电子式为、化合物D形成的晶体属于(填“原子晶体”、“分子晶体”或“离子晶体”)。
(3)单质甲和化合物C反应的化学方程式为。
(4)化合物的B和化合物D反应的化学方程式为。
某芳香烃A有如下转化关系: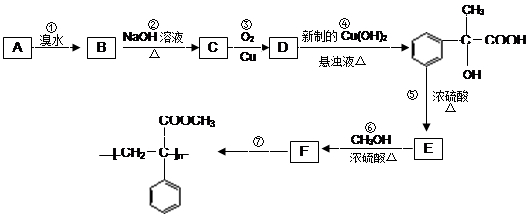
按要求填空:
⑴写出反应①的反应类型;
⑵写出A和F结构简式:A;F;
⑶写出反应③和⑤的化学方程式:
③,
⑤。
中国一贯反对使用化学武器,反对任何形式的化学武器扩散。苯氯乙酮是一种具有荷花香味且有强催泪作用的杀伤性化学毒剂,它的结构简式为:
试回答下列问题:
(1)苯氯乙酮不可能发生的化学反应是__________ (填序号)。
| A.加成反应 | B.取代反应 | C.消去反应 | D.银镜反应 |
(2)与苯氯乙酮互为同分异构体,且能发生银镜反应,分子中有苯环但不含—CH3的化合物有多种,它们的结构简式是:
还有__________;__________;__________;__________;__________。
(根据本题要求,必须写全同分异构体,但不一定填满。)