为探索工业含铝、铁、铜合金废料的再利用,甲同学设计的实验方案如下: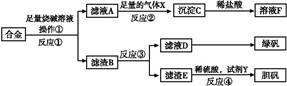
请回答:
(1)操作①用到的玻璃仪器有 。
(2)写出反应①的化学方程式: ,反应②的离子反应方程式: 。
(3)设计实验方案,检测滤液D中含有的金属离子(试剂自选) 。
(4)在滤渣E中加入稀硫酸和试剂Y制胆矾晶体是一种绿色化学工艺,试剂Y为无色液体,反应④的总化学方程式是 。
(5)乙同学在甲同学方案的基础上提出用滤渣B来制备FeCl3·6H2O晶体,在滤渣中滴加盐酸时,发现反应速率比同浓度盐酸与纯铁粉反应要快,其原因是 。
将所得氯化铁溶液用加热浓缩、降温结晶法制得FeCl3·6H2O 晶体,而不用直接蒸发结晶的方法来制得晶体的理由是 。
(6)将滤渣B的均匀混合物平均分成四等份,分别加入同浓度的稀硝酸,充分反应后,在标准状况下生成NO的体积与剩余金属的质量见下表(设硝酸的还原产物只有NO)。
| 实验编号 |
① |
② |
③ |
④ |
| 稀硝酸体积(mL) |
100 |
200 |
300 |
400 |
| 剩余金属质量(g) |
9.0 |
4.8 |
0 |
0 |
| NO体积(L) |
1.12 |
2.24 |
3.36 |
V |
则硝酸的浓度为 ;③中溶解铜的质量为 ;④中V= 。
A、B、C、D、E五种短周期元素,它们的原子序数依次增大;A元素是原子半径最小的原子;B元素的最高价氧化物对应水化物与其氢化物生成一种盐X;D与A同主族,且与E同周期;E元素的最外层电子数是其次外层电子数的3/4,A、B、D、E这四种元素,每一种与C元素都能形成元素的原子个数比不相同的若干种化合物。请回答下列问题:
(1)C和E两元素相比较,非金属性较强的是 (填元素名称),可以验证该结论的是 (填写编号)
A.比较这两种元素的气态氢化物的沸点
B.比较这两种元素的原子的电子层数
C.比较这两种元素的气态氢化物的稳定性
D.比较这两种元素的单质与氢化合的难易
(2)C、D两元素形成的原子个数比为1:1的化合物与C、E两元素形成的两种化合物都能反应,且有一种共同的产物,写出这两个反应的化学方程式:;。
(3)某工业生产的核心反应是 :2EC2(g)+ C2(g)  2EC3(g)△H<0,回答下列问题:
2EC3(g)△H<0,回答下列问题:
①此反应的平衡常数表达式为K=,随着温度的升高,上述平衡常数
(填“增大”、“减小”或“不变”)。
②将一定量的EC2(g)和C2(g)放入1L密闭容器中,在一定条件下达到平衡,测得EC2为0.11mol,C2为0.05mol,EC3为0.12mol。计算该条件下,反应的平衡常数K=。EC2的转化为EC3转化率=。
(4)A、C、E间可形成甲、乙两种微粒,它们均为负一价双原子阴离子,且甲有18个电子,乙有10个电子,则甲与乙反应的离子方程式为;
(5)①在火箭推进器中装有液态B2A4和液态A2C2,已知0.4mol.液态B2A4和足量液态A2C2反应,生成气态B2和气态A2C,放出256.6kJ的热量。试写出该反应的热化学方程式:。
②B2A4又称为肼,是一种可燃性液体,肼一空气燃料电池是一种碱性燃料电池,电解质溶液是20%—30%的KOH溶液,该电池放电时的电极反应式为:正极,负极
取1.43 g Na2CO3•xH2O溶于水配成10mL溶液,然后逐滴滴入稀盐酸直至没有气体放出为止,用去盐酸2.0mL,并收集到112mLCO2(标况)。
求:(1)稀盐酸物质的量浓度为mol•L-1
(2)Na2CO3•xH2O的摩尔质量为g•mol-1
(3)x=
下图表示在没有通风橱的条件下制备氯气时设计的装置,图中a、b是可控制的弹簧铁夹。(氯气在饱和氯化钠溶液中的溶解度较小。)
(1)仪器A的名称是;水槽中应盛放的是;烧杯中盛放的是;烧瓶中反应的化学方程式;
在收集氯气时,应打开关闭 (填a, b)当氯气收集完毕,尾气处理时烧杯中发生反应的离子方程式。
写出下列化学方程式、离子方程式或电离方程式:
(1)碳酸钠溶液和过量的醋酸溶液反应(离子方程式)
(2)镁在二氧化碳气体中燃烧(化学方程式)
(3)次氯酸电离(电离方程式)
趣小组在课外活动中,对某溶液进行了多次检测,其中三次检测结果如下表所示,请回答:
| 检测次数 |
溶液中检测出的物质 |
| 第一次 |
KCl、K2SO4、Na2CO3、NaCl |
| 第二次 |
KCl、BaCl2、Na2SO4、K2CO3 |
| 第三次 |
Na2SO4、KCl、K2CO3、NaCl |
(1)三次检测结果中第次检测结果不正确。
(2)在检测时,为了确定溶液中是否存在硫酸根离子、碳酸根离子和氯离子(提示:Ag2SO4微溶于水):
第一步:向溶液中滴加过量的溶液,其目的是检验CO32-。并将其除去;
第二步:加入过量的Ba(NO3)2,其目的是;
第三步:过滤,再向滤液中加入溶液(填化学式),发生反应的离子方程式。