如图所示是验证氯气性质的微型实验,a、b、d、e是浸有相关溶液的滤纸。向KMnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面。已知:2KMnO4+16HCl=2KCl+5Cl2↑+2MnCl2+8H2O。对实验现象的“解释或结论”正确的是( )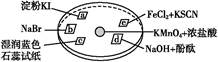
| 选项 |
实验现象 |
解释或结论 |
| A |
a处变蓝,b处变红棕色 |
氧化性:Cl2>Br2>I2 |
| B |
c处先变红,后褪色 |
氯气与水生成了酸性物质 |
| C |
d处立即褪色 |
氯气与水生成了漂白性物质 |
| D |
e处变红色 |
还原性:Fe2+>Cl- |
将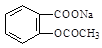 转变为
转变为 的方法为:
的方法为:
| A.与足量的NaOH溶液共热后,再通入CO2 | B.溶液加热,通入足量的HCl |
| C.与稀H2SO4共热后,加入足量的Na2CO3 | D.与稀H2SO4共热后,加入足量的NaOH |
现有三组混合液:(1)甲酸乙酯和乙酸钠;(2)乙醇和丁醇;(3)溴化钠和单质溴的水溶液分离以上各混合液的正确方法依此是
| A.分液、萃取、蒸馏 | B.萃取、分液、蒸馏 |
| C.萃取、蒸馏、分液 | D.分液、蒸馏、萃取 |
相同温度下,在体积相等的三个恒容密闭容器中发生可逆反应: N2(g) + 3H2(g)  2NH3(g) △H=-92.4 kJ/mol。
2NH3(g) △H=-92.4 kJ/mol。
实验测得起始、平衡时的有关数据如下表:
| 容器编号 |
起始时各物质物质的量/mol |
平衡时反应中的能量变化 |
||
| N2 |
H2 |
NH3 |
||
| ① |
1 |
3 |
0 |
放出热量a kJ |
| ② |
2 |
3 |
0 |
放出热量b kJ |
| ③ |
2 |
6 |
0 |
放出热量c kJ |
下列叙述正确的是 ()
A.放出热量关系:a < b < 92.4
B.三个容器内反应的平衡常数:③ > ① > ②
C.达平衡时氨气的体积分数:① > ③
D.N2的转化率:② > ① > ③
下列物质中,既能与硫化氢反应又能使溴水褪色的是()
①硫化钾溶液②二氧化硫③硫酸铜溶液④硝酸银溶液⑤小苏打溶液⑥烧碱溶液
| A.①②③ | B.①②④⑤⑥ | C.③④⑤⑥ | D.②④⑥ |
下列各组物质间反应可能包括多步反应,其总的离子方程式正确的是()
| A.在硫酸工艺流程中,对尾气中的SO2用过量的氨水吸收的反应 2 NH3·H2O + SO2= 2NH4++ SO32-+H2O |
| B.FeCl2在空气中被氧化 4Fe2+ + O2 + 2H2O = 4Fe3+ + 4OH- |
| C.AlCl3溶液中通入过量的NH3:Al3++4NH3·H2O=AlO2-+4NH4+ |
| D.FeBr2 (aq) 中通入少量Cl2 2Fe2+ + 4Br— + 3Cl2 = 2Fe3+ + 2 Br2 + 6Cl— |