某芳香族化合物A苯环上只有一个取代基,发生的反应如图所示,B、F、G的分子式分别为C2H4O2、H2C2O4、C6H12O,H能使溴水褪色。
(1)A的结构简式 ,H的键线式 。
(2)B中的官能团名称为 ,⑤的反应类型为 。
(3)C在一定条件下形成高分子化合物的化学方程式 。
(4)足量G与F反应的化学方程式 。
(5)G的同分异构体中能发生银镜反应的共有 种,其中核磁共振氢谱有三组特征峰的有机物结构简式为 。
乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物。完成下列各题:
(1)正四面体烷的分子式为,其二氯取代产物有种;
(2)关于乙烯基乙炔分子的说法错误的是:
a.能使酸性KMnO4溶液褪色
b.1摩尔乙烯基乙炔能与3摩尔Br2发生加成反应
c.生成乙烯基乙炔分子的反应属于取代反应
d.等质量的乙炔与乙烯基乙炔完全燃烧时的耗氧量不相同
(3)写出与环辛四烯互为同分异构体且属于芳香烃的分子的结构简式:
(4)写出与苯互为同系物且一氯代物只有两种的物质的结构简式(举两例):、
有下列反应:①由乙烯制乙醇②甲烷在空气中燃烧
③由乙炔制氯乙烯④丙烯使溴水褪色 ⑤苯与浓硝酸、浓硫酸的混合酸反应⑥用丙烯制聚丙烯
其中属于取代反应的是(填序号,下同),属于氧化反应的是,
属于加成反应的是,属于加聚反应的是。
为除去粗盐中的Ca2+、Mg2+、Fe3+、SO以及泥沙等杂质,一位同学设计了一种制备精盐的实验方案,步骤如下(用于生成沉淀的试剂均稍过量):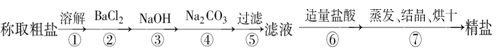
(1)判断BaCl2已过量的方法是______________________________。
(2)第④步中,相关的离子方程式是_________________________________。
(3)蒸发、结晶时,当时停止加热。
实验室用NaOH固体配制250mL 1.25mol/L的NaOH溶液,填空并请回答下列问题:
(1)配制250mL 1.25mol/L的NaOH溶液
| 应称取NaOH的质量/g |
应选用容量瓶的规格/mL |
除容量瓶外还需要的其它玻璃仪器 |
(2)容量瓶上需标有以下五项中的;
①温度 ②浓度 ③容量 ④压强 ⑤刻度线
(3)配制时,其正确的操作顺序是(字母表示,每个字母只能用一次);
A、用30mL水洗涤烧杯2—3次,洗涤液均注入容量瓶,振荡
B、用天平准确称取所需的NaOH的质量,加入少量水(约30mL),用玻璃棒慢慢搅动,使其充分溶解
C、将已冷却的NaOH溶液沿玻璃棒注入250mL的容量瓶中
D、将容量瓶盖紧,颠倒摇匀
E、改用胶头滴管加水,使溶液凹面恰好与刻度相切
F、继续往容量瓶内小心加水,直到液面接近刻度1—2cm处
(4)操作A中,将洗涤液都移入容量瓶,其目的是,溶液注入容量瓶前需恢复到室温,这是因为_____________________________;
选择下列实验方法分离物质,将分离方法的序号填在横线上。
| A.萃取分液法 |
| B.加热分解 |
| C.结晶法 |
| D.分液法 |
E.蒸馏法
F.过滤法
(1)分离饱和食盐水和沙子的混合物:;
(2)从硝酸钾和氯化钠的混合溶液中获得硝酸钾:;
(3)分离水和油的混合物:;
(4)分离CCl4(沸点:76.75℃)和甲苯(沸点:110.6℃)的混合:;
(5)从碘的水溶液中提取碘:。