(届上海市杨浦区第一学期期末试题)实验室需配置一定浓度的硝酸钾溶液。
(1)查阅硝酸钾溶解性。由右图可知,20℃时,硝酸钾的溶解度为________g,在该温度下配制硝酸钾溶液,溶质质量分数最大为____%(计算结果保留整数)。
(2)计算。配制40 g质量分数为10%的硝酸钾溶液,所需硝酸钾质量为________g,所需蒸馏水的体积为________mL(水的密度近似看做l g/mL)。
(3)称量。分别在天平左右两盘放上纸片,调节平衡后,________(填字母)。
A.先移动游码到所需位置,再添加硝酸钾直到天平平衡
B.先添加所需的硝酸钾,再移动游码直到天平平衡
(4)量取。量取所需蒸馏水要用到的仪器是____(填字母)。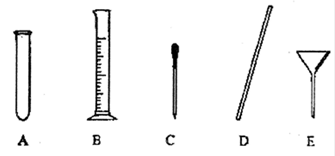
(5)溶解。将称量好的硝酸钾和蒸馏水混合溶解。
(6)稀释。20℃时,将20 mL质量分数为10%的硝酸钾溶液,稀释成质量分数为4%的硝酸钾溶液。从下表中找出需要用到的数据:____________g/mL。
硝酸钾溶液的密度(单位1 g/rnL)
| 温度℃ 质量分数/% |
20 |
40 |
60 |
| 4 |
1.023 |
1.016 |
1.007 |
| 10 |
1.063 |
1.054 |
1.004 |
(7)20℃时,取哪份定质量的饱和硝酸钾溶液进行如下实验后,所得结论正确的是________。
A.保持温度不变,减少10 g溶剂后,溶液中溶质的质量分数增大
B.保持温度不变,加入10 g溶质后,溶液中溶质的质量分数增大
C.保持温度不变,加入10 g溶剂后,溶质的溶解度减小
D.降温至10℃后,溶质的溶解度减小
化学与生活息息相关,可以帮助人类认识、改造世界。
(1)减少煤、和天然气等化石燃料的燃烧,会有助于减少二氧化碳的产生和雾霾天气的发生。
(2)目前,人们正在利用和开发新能源,如太阳能、核能、地热能、能等。
(3)下列说法正确的是(填序号)
①把秸杆、杂草等废弃物放在密闭池中发酵可以产生沼气
②点燃沼气与空气的混合气体可能发生爆炸
③随着人类对能源的需求量日益增长,不可再生能源将面临枯竭的危险
④人类利用的能量都是通过化学反应获得的
(4)农家院食品有鱼、大米、黑木耳、山野菜等,这些食品深受游客喜爱,其中富含糖类的是。
(5)NaOH的俗称是,它可用于制备消毒剂(NaClO),其中Cl元素的化合价是 。
(6)元素对人体健康的影响很大。例如,缺元素可能引起佝偻病。
下图是配制50g溶质质量分数为6%的氢氧化钠溶液的有关操作示意图: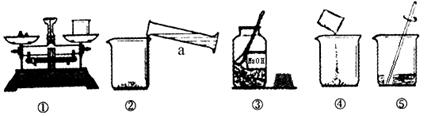
(1)仪器a的名称:__________________;
(2)①②③④⑤步中有一步是错误的,它是_______________(填序号);
将错误操作改正后,用上述序号表示正确操作顺序是_______________;
(3)计算需要氢氧化钠______________g;
(4)若用量筒量取水时仰视读数,其他操作正确,则配得的溶液中氢氧化钠的质量分数____________(填“偏大”“偏小”或“正确”)。
每到冬天,市场上便有一种“热宝”出售,它是一个装有化学药品的小袋。使用时,撕去它的保护膜贴在身体上,不久便会产生热量。已知小袋中装有铁粉、碳粉和少量氯化钠。
(1)“热宝”使用前,取小袋内物质,加入稀硫酸中,发生反应的化学方程式为:
_________________________________________________________________________;
(2)“热宝”发热,其实是利用了铁粉与空气中的___________________反应放出的热量。“热宝”工作一段时间后失效,此时取小袋内物质,加入一定量的稀硫酸写出反应的化学方程式_________________________________________________,充分反应后过滤,则滤液中一定有的溶质是____________________(填写化学式)。
下图是某实验小组的同学绘制的两种固体物质的溶解度曲线图。请你根据图示回答问题:
(1)t1℃时,甲物质的溶解度_________乙物质的溶解度(填“>”“<”或“=”)。P点代表的意义 ;
(2)溶解度曲线图中的任何一点都表示溶液的一种特定状态。图中A、B两个状态中,溶液属于不饱和状态的是______________;
(3)在t1℃时,将相同质量的甲、乙两种物质饱和溶液,分别升温到t2℃,此时,甲溶液的含水量__________乙溶液的含水量(填“>”“<”或“=”)。
硬水会给我们的生活和生产带来很多危害,如用硬水洗衣物既浪费肥皂,也洗不净衣物;烧锅炉时用硬水易使锅炉内结水垢,不仅浪费燃料,严重时可能引起爆炸;人长期饮用硬水可能会得结石。
下列能降低水的硬度方法是(填序号);
①过滤②加活性炭③煮沸 ④加消毒剂
在学校开展研究性学习时,某同学提出可以用稀盐酸除去水垢(主要成分是Mg(OH)2和CaCO3),请写出相关的化学反应方程式:
___________________________________;___________________________________。