下列化学实验事实及其结论都正确的是( )
| 选项 |
实验事实 |
结论 |
| A |
将SO2通入含HClO的溶液中生成H2SO4 |
HClO的酸性比H2SO4强 |
| B |
铝箔在酒精灯火焰上加热熔化但不滴落 |
铝箔表面氧化铝熔点高于铝 |
| C |
SiO2可以和NaOH溶液及HF溶液反应 |
SiO2属于两性氧化物 |
| D |
将SO2通入溴水中,溴水褪色 |
SO2具有漂白性 |
将14g铜银合金跟足量的某浓度HNO3反应,将放出的气体与1.12LO2(标准状况)混合,通入水中,恰好全部吸收,则合金中银的质量是
| A.3.2g | B.10.8g | C.21.6g | D.5.4g |
关于硝酸的说法正确的是
| A.硝酸电离出的H+离子,能被Zn、Fe等金属还原成H2 |
| B.常温下,向浓HNO3中投入Fe片,会产生大量的红棕色气体 |
| C.硝酸与金属反应时,主要是+5价的氮得电子 |
| D.浓HNO3与浓HCl按3∶1的体积比所得的混合物叫王水 |
下表为元素周期表的一部分,参照元素①~⑦在表中的位置,请用化学用语回答下列问题: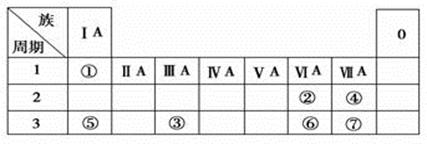
(1)④、⑤、⑦的原子半径由大到小的顺序为(用化学用语表示,下同)。
(2)⑥和⑦的最高价含氧酸的酸性强弱为。
(3)①、②两种元素按原子个数之比为1:1组成的常见液态化合物,在酸性溶液中能将Fe2+氧化,写出该反应的离子方程式 。
(4)由表中元素形成的物质可发生如图中的反应,其中B、C、G是单质,B为黄绿色气体,D溶液显碱性。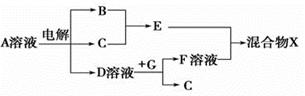
①写出D溶液与G反应的化学方程式:。
②写出检验A溶液中溶质的阴离子的方法:。
③常温下,若电解1 L 0.1 mol/L的A溶液,一段时间后测得溶液中的c(OH - ) =10-2 mol/L (忽略溶液体积变化),则该电解过程中转移电子的物质的量为 mol。
在电解食盐水之前,需要提纯食盐水。为了除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,可将粗盐溶于水,然后进行下列五项操作:①过滤,②加过量的NaOH溶液,③加适量的盐酸,④加过量的碳酸钠溶液,⑤加过量的氯化钡溶液。正确的操作顺序是
| A.①④②⑤③ | B.④①②⑤③ | C.②⑤④①③ | D.⑤②④③① |
海水中含有MgCl2,从海水中提取镁,正确的方法是
A.海水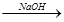 Mg(OH)2 Mg(OH)2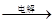 Mg Mg |
B.海水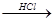 MgCl2溶液→ MgCl2(熔融) MgCl2溶液→ MgCl2(熔融)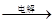 Mg Mg |
C.海水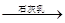 Mg(OH)2 Mg(OH)2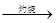 MgO MgO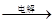 Mg Mg |
D.海水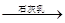 Mg(OH)2 Mg(OH)2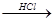 MgCl2溶液 → MgCl2(熔融) MgCl2溶液 → MgCl2(熔融)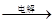 Mg Mg |