NaNO2是一种食品添加剂,它能致癌。酸性KMnO4溶液与NaNO2的反应方程是:MnO4—+NO2—+ 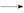 Mn2++NO3—+H2O(未配平)。下列叙述中正确的是( )
Mn2++NO3—+H2O(未配平)。下列叙述中正确的是( )
| A.该反应中NO2—被还原 |
| B.反应过程中溶液的pH减小 |
| C.生成1 mol NaNO3需消耗0.4 mol KMnO4 |
| D.中的粒子是OH- |
在一定温度下,对于可逆反应C(s)+H2O(g) 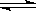 CO(g)+H2(g),其平衡常数表达式正确的是()
CO(g)+H2(g),其平衡常数表达式正确的是()
A.K=[c(C)·c(H2O)]/ [c(CO)·c(H2)] B.K= [c(CO)·c(H2)]/ [c(C)·c(H2O)]
C.K=[c(H2O)]/ [c(CO)·c(H2)]D.K=[c(CO)·c(H2)/ [c(H2O)]]
下列变化过程中,需要吸热的是()
| A.生石灰与水混合 | B.天然气燃烧 |
| C.浓硫酸溶于水 | D.干冰气化 |
下列物质中,属于弱电解质的是()
| A.氯化氢 | B.氢氧化钠 | C.一水合氨 | D.酒精 |
一种气态烷烃和气态烯烃组成的混合物10g,其密度为相同条件下氢气密度的12.5倍,该混合气体通过溴水,使溴水增重8.4g,则混合气体为()
| A.甲烷和丙烯 | B.乙烷和乙烯 | C.甲烷和乙烯 | D.乙烷和丙烯 |
已知酸性强弱顺序为H2CO2> >HCO3—,下列化学方程式正确的是()
>HCO3—,下列化学方程式正确的是()
A. +H2O+CO2→ +H2O+CO2→ +Na2CO3 +Na2CO3 |
B. +H2O→ +H2O→ +NaOH +NaOH |
C. +Na2CO3→ +Na2CO3→ +NaHCO3 +NaHCO3 |
D. +NaHCO3→ +NaHCO3→ +H2CO3 +H2CO3 |