已知 水杨酸酯E为紫外线吸收剂,可用于配制防晒霜。E的一种合成路线如下:
水杨酸酯E为紫外线吸收剂,可用于配制防晒霜。E的一种合成路线如下:
请回答下列问题:
(1)一元醇A中氧的质量分数约为21.6%。则A的分子式为 。结构分析显示A只有一个甲基.A的名称为 。
(2)B能发生银镜反应,该反应的化学方程式为 。
(3)C有 种结构;若一次取样,检验C中所含官能团,按使用的先后顺序写出所用试剂 。
(4)第③步的反应类型为 ;D所含官能团的名称为 。
(5)写出同时符合下列条件的水杨酸的同分异构体的结构简式:(任写一种) 。
a.分子中含有6个碳原子在一条线上;
b.分子中所含官能团包括水杨酸具有的官能团
(6)写出E的结构简式 。
正极材料为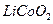 的锂离子电池已被广泛用作便携式电源。但钴的资源匮乏限制了其进一步发展。
的锂离子电池已被广泛用作便携式电源。但钴的资源匮乏限制了其进一步发展。
(1)橄榄石型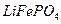 是一种潜在的锂离子电池正极材料,它可以通过
是一种潜在的锂离子电池正极材料,它可以通过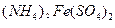 、
、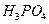 与
与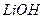 溶液发生共沉淀反应,所得沉淀经80℃真空干燥、高温成型而制得。
溶液发生共沉淀反应,所得沉淀经80℃真空干燥、高温成型而制得。
①共沉淀反应投料时,不将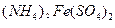 和
和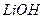 溶液直接混合的原因是。
溶液直接混合的原因是。
②共沉淀反应的化学方程式为。
③高温成型前,常向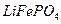 中加入少量活性炭黑,其作用除了可以改善成型后的
中加入少量活性炭黑,其作用除了可以改善成型后的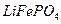 的导电性能外,还能。
的导电性能外,还能。
(2)废旧锂离子电池的正极材料试样(主要含有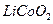 及少量AI、Fe等)可通过下列实验方法回收钴、锂。
及少量AI、Fe等)可通过下列实验方法回收钴、锂。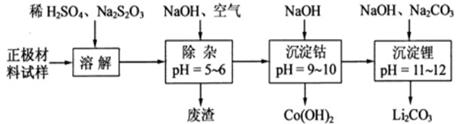
①在上述溶解过程中,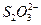 被氧化成
被氧化成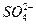 ,
,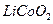 在溶解过程中反应的化学方程式为。
在溶解过程中反应的化学方程式为。
②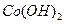 在空气中加热时,固体残留率随温度的变化,如下图所示。已知钴的氢氧化物加热至290℃时已完全脱水,则1000℃时,剩余固体的成分为。(填化学式);在350~400℃范围内,剩余固体的成分为。(填化学式)。
在空气中加热时,固体残留率随温度的变化,如下图所示。已知钴的氢氧化物加热至290℃时已完全脱水,则1000℃时,剩余固体的成分为。(填化学式);在350~400℃范围内,剩余固体的成分为。(填化学式)。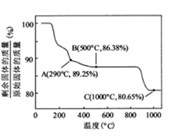
下表列出了3种燃煤烟气脱硫方法的原理。
(1)方法Ⅰ中氨水吸收燃煤烟气中 的化学反应为:
的化学反应为: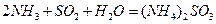

能提高燃煤烟气中 去除率的措施有__________(填字母)。
去除率的措施有__________(填字母)。
A.增大氨水浓度 B.升高反应温度
C.使燃煤烟气与氨水充分接触 D . 通入空气使
. 通入空气使 转化为
转化为
采用方法Ⅰ脱硫,并不需要预先除去燃煤烟气中大量的 ,原因是▲(用离子方程式表示)。
,原因是▲(用离子方程式表示)。
(2)方法Ⅱ重要发生了下列反应:
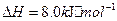






 与
与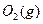 反应生成
反应生成 的热化学方程式为
的热化学方程式为 。
。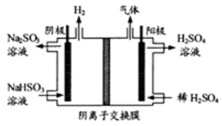
(3)方法Ⅲ中用惰性电极电解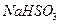 溶液的装置如上图所示。阳极区放出气体的成分为。(填化学式)
溶液的装置如上图所示。阳极区放出气体的成分为。(填化学式)
以水氯镁石(主要成分为 )为原料生产碱式碳酸镁的主要流程如下:
)为原料生产碱式碳酸镁的主要流程如下:
(l)预氨化过程中有Mg(OH)2沉淀生成,已知常温下Mg(OH)2的 ,若溶液中
,若溶液中 ,则溶液中
,则溶液中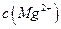 = 。
= 。
(2)上述流程中的滤液浓缩结晶,所得主要固体物质的化学式为 。
。
(3)高温煅烧碱式碳酸镁得到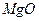 。取碱式碳酸镁4.66g,高温煅烧至恒重,得到固体2.00g和标准状况下
。取碱式碳酸镁4.66g,高温煅烧至恒重,得到固体2.00g和标准状况下 0.896L,通过计算确定碱式碳酸镁的化学式。
0.896L,通过计算确定碱式碳酸镁的化学式。
(4)若热水解不完全,所得碱式碳酸镁中将混有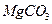 ,则产品中镁的质量分数▲ (填 “升高”、“降低”或“不变”)。
,则产品中镁的质量分数▲ (填 “升高”、“降低”或“不变”)。
钡盐行业生产中排出大量的钡泥[主要含有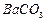 、
、 、
、 、
、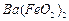 等。某主要生产
等。某主要生产 、
、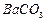 、
、 的化工厂利用钡泥制取
的化工厂利用钡泥制取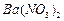 ,其部分工艺流程如下:
,其部分工艺流程如下: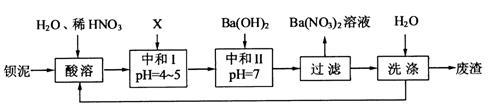
(1)酸溶后溶液中 ,
,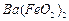 与
与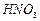 的反应化学方程式为 。
的反应化学方程式为 。
(2)酸溶时通常控制反应温度不超过70℃,且不使用浓硝酸,
原因是 、 。
(3)该厂结合本厂实际,选用的X为 (填化学式);中和Ⅰ使溶液中 (填离子符号)的浓度减少(中和Ⅰ引起的溶液体积变化可忽略)。
(4)上述流程中洗涤的目的是 。

上图中
均为有机化合物,根据图中的信息,回答下列问题:
(1)环状化合物
的相对分子质量为82,其中含碳87.80%,含氢12.20%。
的一氯代物仅有一种,
的结构简式为;
(2)
是
的一种同分异构体,
能使溴的四氯化碳溶液褪色,分子中所有的碳原子共平面,则
的结构简式为;
(3)由
生成
的反应类型是,由
生成
的反应类型是;
(4)
的分子式为
,0.146g
需用
溶液完全中和,
是一种高分子化合物。则由
转化为
的化学方程式为;
(5)分子中含有两个碳碳双键,且两个双键之间有一个碳碳单键的烯烃与单烯烃可发生如下反应
则由
和
反应生成F的化学方程式为;
(6)
中含有的官能团是,
中含有的官能团是。