 的正确名称是( )
的正确名称是( )
A.2,5 二甲基 二甲基 4 4 乙基己烷 乙基己烷 |
B.2,5 二甲基 二甲基 3 3 乙基己烷 乙基己烷 |
C.3 异丙基 异丙基 5 5 甲基己烷 甲基己烷 |
D.2 甲基 甲基 4 4 异丙基己烷 异丙基己烷 |
下列微粒中,对水的电离平衡不产生影响的是
A.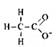 |
B. |
C. |
D.1s22s22p63s1 |
很多国家已停止使用含铊的杀虫剂。元素周期表中铊的数据见右图,下列说法正确的是
| A.TI元素是一种主族元素 |
| B.TI元素的相对原子质量是204 |
| C.铊元素的质量数是204.4 |
| D.TI原子最外层有3个能量相同的电子 |
根据碘与氢气反应的热化学方程式
(i)I2(g)+ H2(g)  2HI(g)+ 9.48 kJ (ii) I2(s)+ H2(g)
2HI(g)+ 9.48 kJ (ii) I2(s)+ H2(g) 2HI(g) - 26.48 kJ
2HI(g) - 26.48 kJ
下列判断正确的是
| A.1mol I2(s)中通入2gH2(g),反应吸热26.48 kJ |
| B.1 mol固态碘与1 mol气态碘所含的能量相差17.00 kJ |
| C.反应(ii)的反应物总能量比反应(i)的反应物总能量低 |
| D.反应(i)放出的热量多,所以产物的能量低,比反应(ii)的产物更稳定 |
在生产和生活中金属腐蚀难以避免。对图a和图b的分析合理的是
| A.图a,负极上发生的反应是:O2+4e+2H2O → 4OH- |
| B.图b,接通开关后溶液中的H+向正极移动 |
| C.图a,插入海水中的铁棒,越靠近底端腐蚀越严重 |
| D.图b,接通开关后Zn腐蚀速率增大,Zn上放出气体的速率也增大 |
证明苯酚分子里羟基上的氢原子比乙醇分子里羟基上的氢原子活泼的事实是
A.苯酚能与浓溴水发生取代反应,而乙醇不能
B苯酚能与氢氧化钠反应,而乙醇不能
C常温下,苯酚微溶于水,而乙醇与水互溶
D.苯酚有毒,而乙醇无毒