现有七种短周期主族元素,其原子序数按A、B、C、D、E、F、G的顺序递增。A元素的最高正化合价和最低负化合价的代数和等于0,且A是形成化合物种类最多的元素;C原子能形成分别含10电子、18电子的两种阴离子,且C与F位于同一主族;D单质投入冷水中反应缓慢,投入沸水中迅速产生气泡;E的简单阳离子是同周期元素所形成的简单离子中半径最小的。回答下列问题:
(1)B位于周期表第________周期第________族。
(2)A、B、C三种元素能形成等电子体,请写出其中一组等电子体:________________________________________________________________________。
(3)元素M位于E与F元素之间,且M单质是优良的半导体材料,广泛用于太阳能电池。M、F、G的气态氢化物的稳定性由强到弱的顺序为______________(用化学式表示)。
(4)若选择三种试剂设计实验能证明非金属性:B>A>M,用化学方程式表示实验原理:__________________________________________________。
(5)A、M、F、G的最高价氧化物对应水化物的酸性由强到弱的顺序为________________________(用化学式表示)。
(6)下列实验方法能证明D与E的金属性强弱关系的是________(填字母序号)。
A.比较D和E的单质分别与稀硫酸反应产生气泡的快慢
B.比较D和E的单质分别与同浓度的氢氧化钠溶液反应产生气泡的快慢
C.比较D和E的单质分别与氯气、氧气、硫等非金属单质反应的产物
元素在周期表中的位置,反映了元素的原子结构和元素的性质。右图是元素周期表的一部分。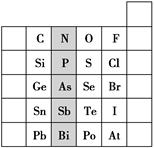
(1)阴影部分元素在元素周期表中的位置为________族。
(2)根据元素周期律预测:H3AsO4属于强酸还是弱酸?________。
(3)C和Si元素的氢化物都可以燃烧,但Si元素的氢化物在空气中可以自燃,其原因是_________________________________________。
试写出Si的氢化物完全燃烧的化学方程式:______________________________。
(4)O2与H2的反应是不可逆反应,而S与H2反应有一定限度,请写出Se与H2反应的化学方程式:______________________
(5)试比较S、O、F三种元素的原子半径大小:________(填元素符号)。
(1)X元素的原子核外有2个电子层,其中L层有5个电子,该元素在周期表中的位置为________,最高价氧化物的化学式为________,该元素的氢化物和最高价氧化物对应水化物反应的化学方程式为______________________
(2)Y为短周期元素,若其最高价氧化物对应水化物的化学式为HYO3,则此时Y元素的化合价为________,Y原子的最外层电子数为________,其气态氢化物的化学式为__________________。
下列关于元素周期律和元素周期表的论述中正确的是( )。
| A.同一主族的元素从上到下金属性逐渐减弱 |
| B.元素周期表是元素周期律的具体表现形式 |
| C.同一周期从左到右,元素原子半径逐渐增大 |
| D.非金属元素的最高正化合价等于它的负化合价的绝对值 |
下表为元素周期表的一部分,请回答有关问题:
| ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
|
| 2 |
① |
② |
||||||
| 3 |
③ |
④ |
⑤ |
⑥ |
⑦ |
⑧ |
||
| 4 |
⑨ |
⑩ |
(1)⑤和⑧的元素符号分别是__________和__________。
(2)表中最活泼的金属是__________,非金属性最强的元素是__________。(填写元素符号)
(3)表中能形成两性氢氧化物的元素是__________,分别写出该元素的氢氧化物与⑥和⑨最高价氧化物的水化物反应的化学方程式:______________________________, ________________________________。
(4)请设计一个实验,比较⑦⑩单质氧化性的强弱:
_________________________________________________________________。
A、B、C、D四种短周期元素,原子序数D>A>B>C,且A、B同周期,C、D同主族,A的原子结构示意图为: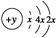 ,B最外层电子数是2,C的气态氢化物的水溶液呈碱性,据此填空:
,B最外层电子数是2,C的气态氢化物的水溶液呈碱性,据此填空:
(1)A的元素名称为________,其气态氢化物的稳定性比CH4________(填“强”或“弱”)。
(2)C、D的最高价氧化物的水化物的酸性大小为________>________(填化学式)。
(3)B的活泼性比钙的________(填“强”或“弱”)。