工业上合成氨的反应:N2(g)+3H2(g)  2NH3(g)ΔH=-92.60 kJ·mol-1。
2NH3(g)ΔH=-92.60 kJ·mol-1。
(1)在绝热、容积固定的密闭容器中发生反应:N2(g)+3H2(g)  2NH3(g),下列说法能说明上述反应向正反应方向进行的是________(填序号)。
2NH3(g),下列说法能说明上述反应向正反应方向进行的是________(填序号)。
①单位时间内生成2n mol NH3的同时生成3n mol H2
②单位时间内生成6n mol N—H键的同时生成2n mol H—H键
③用N2、H2、NH3的物质的量浓度变化表示的反应速率之比为1∶3∶2
④混合气体的平均摩尔质量增大
⑤容器内的气体密度不变
(2)已知合成氨反应在某温度下2 L的密闭容器中进行,测得如下数据:
| 时间(h) 物质的量(mol) |
0 |
1 |
2 |
3 |
4 |
| N2 |
1.50 |
n1 |
1.20 |
n3 |
1.00 |
| H2 |
4.50 |
4.20 |
3.60 |
n4 |
3.00 |
| NH3 |
0 |
0.20 |
|
1.00 |
1.00 |
根据表中数据计算:
①反应进行到2 h时放出的热量为________ kJ。
②0~1 h内N2的平均反应速率为________ mol·L-1·h-1。
③此温度下该反应的化学平衡常数K=________(保留两位小数)。
④反应达到平衡后,若往平衡体系中再加入N2、H2和NH3各1.00 mol,化学平衡将向________方向移动(填“正反应”或“逆反应”)。
化合物A最早发现于酸牛奶中,它是人体内糖代谢的中间体,可由马铃薯、玉米淀粉等发酵制得,A的钙盐是人们喜爱的补钙剂之一。A在某种催化剂的存在下进行氧化,其产物不能发生银镜反应。在浓硫酸存在下,A可发生如下图所示的反应。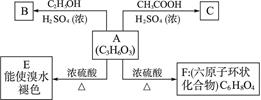
试写出:
(1)化合物A、B、D的结构简式:__________、__________、__________。
(2)化学方程式:A→E____________________,A→F______________________。
(3)反应类型,A→E__________,A→F__________。
某有机物由C、H、O三种元素组成,将该有机物3g充分燃烧生成0.15mol二氧化碳和3.6g水,已知该有机物的蒸汽密度为2.68 g/L(折算成标准状况)。该有机物能与金属钠反应。则:
(1)通过计算求出该有机物的分子式为;
(2)写出该有机物的结构简式为、。
(3)取3g该有机物与金属钠反应,产生H2的体积为(标况下)
(4)将该有机物与浓硫酸共热可制得烯烃,请写出反应方程式
(1)  中含氧官能团的结构简式是;该有机物发生加聚反应后,所得产物的结构简式为。
中含氧官能团的结构简式是;该有机物发生加聚反应后,所得产物的结构简式为。
(2) 在酸性条件下水解后生成的有机物为和。
在酸性条件下水解后生成的有机物为和。
(3)写出下列元素的基态原子的核外电子 排布式:
① 35Br______________________________;
② 24Cr ______________________________
以下表格中的实验是以CuSO4为例,分析电解质在溶液里所起反应的实质
(1)下面框图中,A是空气中的一种主要成分,C的相对分子质量比B的大16,D是酸。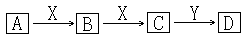
其中A、B、C、D均含有同一元素,请确认B是,X是,Y是。
(2)新制的氯水中存在Cl2、H2O、HClO、HCl,其中能起杀菌消毒作用的是,能与硝酸和硝酸银的混合液作用生成白色沉淀的是,能使染料和有机色质褪色的是。