足量下列物质与等质量的铝反应,放出氢气且消耗溶质物质的量最少的是 ( )
| A.氢氧化钠溶液 | B.稀硫酸 | C.盐酸 | D.稀硝酸 |
下列对有关实验事实的解释正确的是
| A.向某溶液中滴加氯水后,再加入KSCN溶液,溶液呈红色,说明原溶液中含有Fe2+ |
| B.浓硫酸和浓盐酸长期暴露在空气中浓度均降低,原理相同 |
| C.向某溶液中加入氯化钡溶液,生成白色沉淀,再加入稀盐酸,沉淀不溶解,不能说明原溶液一定含有SO42- |
| D.常温下,浓硫酸可以用铁质容器储运,说明铁与冷的浓硫酸不反应 |
足量的两份铝粉分别与等体积的NaOH溶液和稀硫酸反应,同温同压下产生等体积的气体,则NaOH溶液和稀硫酸的物质的量浓度之比为
| A.3:2 | B.2:3 | C.1:3 | D.1:1 |
设NA表示阿伏加德罗常数的值,下列说法错误的是
| A.常温常压下,32gO2和O3的混合气体所含原子数为2NA |
| B.将7.1g氯气通入足量水中发生反应,所转移的电子数为0.1NA |
| C.标准状况下,11.2LSO2中含有的分子数为0.5NA |
| D.23g钠与足量氧气充分反应,转移的电子数一定是NA |
下列能达到实验目的的是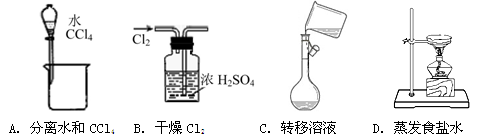
把一定量铁粉放入氯化铁溶液中,完全反应后,所得溶液中Fe2+和Fe3+的物质的量之比为1:2.则已反应的Fe3+和未反应的Fe3+的物质的量之比为
| A.1:1 | B.1:2 | C.1:3 | D.2:3 |