中学常见的某反应的化学方程式为a+b―→c+d+H2O(未配平,反应条件已略去)。
请回答下列问题:
(1)若a是铁,b是稀硝酸(过量),且a可溶于c溶液中。则a与b反应的离子方程式为
___________________________。
(2)若c、d为气体,且都能使澄清石灰水变浑浊,则将此混合气体通入溴水中,橙色褪去,写出其褪色过程中发生反应的离子方程式:___________________________。
(3)若c是无色有刺激性气味的气体,其水溶液显弱碱性,在标准状况下用排空气法收集c气体,得平均摩尔质量为20 g·mol-1的混合气体进行喷泉实验。假设溶质不扩散,实验完成后烧瓶中所得溶液的物质的量浓度为________mol·L-1(小数点后保留2位有效数字)。
(4)若a是造成温室效应的主要气体,c、d均为钠盐,参加反应的a、b的物质的量之比为4:5。则上述反应的离子方程式为____________________________。
请回答钢铁冶炼、腐蚀、防护过程中的有关问题。
(1)工业用热还原法炼铁,写出由CO还原赤铁矿(主要成分为Fe2O3)的化学方程式 。
(2)铁在潮湿的空气中容易被腐蚀为铁锈(Fe2O3•x H2O),写出铁发生电化学腐蚀时负极的电极反应_________ 。
(3)下列各个装置中铁棒被腐蚀由难到易的顺序是____________(填字母)。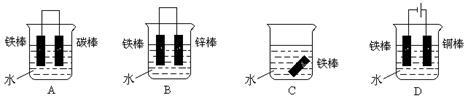
(4)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀。装置如图。请回答: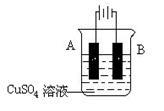
①B电极对应的金属是______(写元素名称),A电极的电极反应式是 。
②若电镀前铁、铜两电极的质量相同,电镀完成后, 若电镀时电路中通过的电子为0.2mol,将它们取出洗净、烘干、称量,则A、B两极质量相差___________ g。
红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g)。反应过程和能量关系如图所示(图中的ΔH表示生成1 mol产物的数据)。根据图回答下列问题:
(1)P和Cl2反应生成PCl3的热化学方程式是 。
(2)PCl5分解成PCl3和Cl2的热化学方程式是 。
(3)P和Cl2分两步反应生成1 mol PCl5的ΔH3=____________,P和Cl2一步反应生成1mol PCl5的ΔH4____ΔH3(填“大于”“小于”或“等于”)。
碳、氮及其化合物在工农业生产生活中有着重要作用。请回答下列问题:
(1)用CH4 催化还原NOx 可以消除氮氧化物的污染。例如:
CH4(g) + 4NO2(g) = 4NO(g)+CO2(g) + 2H2O(g)ΔH1=-574 kJ·mol-1
CH4(g) + 4NO(g) =" 2" N2(g)+CO2(g) + 2H2O(g)ΔH2
若2 mol CH4 还原NO2 至N2,整个过程中放出的热量为1734 kJ,则ΔH2= ;
(2)据报道,科学家在一定条件下利用Fe2O3与甲烷反应可制取“纳米级”的金属铁。其反应如下:Fe2O3(s) + 3CH4(g)  2Fe(s) + 3CO(g) +6H2(g)ΔH>0
2Fe(s) + 3CO(g) +6H2(g)ΔH>0
① 若反应在5L的密闭容器中进行,1min后达到平衡,测得Fe2O3在反应中质量减少3.2g。则该段时间内CO的平均反应速率为 ________________ 。
② 若该反应在恒温恒压容器中进行,能表明该反应达到平衡状态的是_____(选填序号)
a.CH4的转化率等于CO的产率
b.混合气体的平均相对分子质量不变
c.v(CO)与v(H2)的比值不变
d.固体的总质量不变
③ 该反应达到平衡时某物理量随温度变化如图所示,当温度由T1升高到T2时,平衡常数KA ______KB(填“>”、“ <”或“=”)。纵坐标可以表示的物理量有哪些 。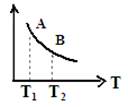
a.H2的逆反应速率
b.CH4的的体积分数
c.混合气体的平均相对分子质量
(3)若往20mL 0.0lmol·L-l的弱酸HNO2溶液中逐滴加入一定浓度的烧碱溶液,测得混合溶液的温度变化如图所示,下列有关说法正确的是________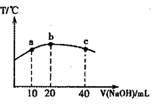
①该烧碱溶液的浓度为0.02mol·L-1
②该烧碱溶液的浓度为0.01mol·L-1
③HNO2的电离平衡常数:b点>a点
④从b点到c点,混合溶液中一直存在:c(Na+)>c(NO2-)>c(OH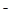 )> c(H+)
)> c(H+)
已知:
以乙炔为原料,通过下图所示步骤能合成有机中间体E(转化过程中反应条件及部分产物已略去).
其中,A、B、C、D分别代表一种有机物;B的化学式为C4H10O2,分子中无甲基.
请回答下列问题:
(1)写出生成A的化学反应方程式:____________.
(2)B在浓硫酸催化下加热,可生成多种有机产物.写出1种相对分子质量比A小的有机产物的结构简式:_______________________.
(3)写出C生成D的化学反应方程式:___________________.
(4)含有苯环,且与E互为同分异构体的酯有______种,写出其中一种同分异构体的结构简式:____________。
M5纤维是美国开发的一种超高性能纤维,下面是M5纤维的合成路线(有些反应未注明条件):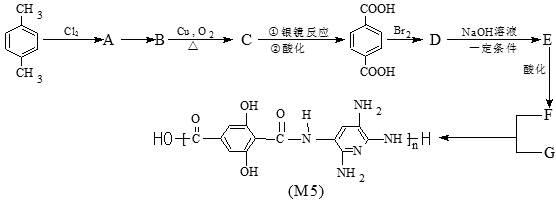
请回答:
(1)写出合成M5的单体F的结构简式:____________________。
(2)反应类型:A→B_________________,F+G→M5___________________________。
(3)某些芳香族有机物是C的同分异构体,则这些芳香族有机物(不包含C)结构中可能有______(填序号)。
a.两个羟基 b.一个醛基 c.两个醛基d.一个羧基
(4)写出化学方程式:B→C_________________
D→E_______________________