下图是实验室制备氯气并进行一系列相关实验的装置(夹持设备已略)。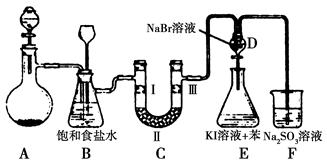
(1)制备氯气选用的药品为漂粉精固体和浓盐酸,相关的化学反应方程式为________。
(2)装置B中饱和食盐水的作用是________;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象:__________________。
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入物质的组合是________(填编号)。
| 编号 |
a |
b |
c |
d |
| Ⅰ |
干燥的有色布条 |
干燥的有色布条 |
湿润的有色布条 |
湿润的有色布条 |
| Ⅱ |
碱石灰 |
硅胶 |
浓硫酸 |
无水氯化钙 |
| Ⅲ |
湿润的有色布条 |
湿润的有色布条 |
干燥的有色布条 |
干燥的有色布条 |
(4)设计装置D、E的目的是比较氯、溴、碘的非金属性。反应一段时间后,打开活塞,将装置D中少量溶液加入装置E中,振荡,观察到的现象是________该现象________(填“能”或“不能”)说明溴的非金属性强于碘,原因是__________________________。
(5)有人提出,装置F中可改用足量的NaHSO3溶液吸收余氯,试写出相应的离子反应方程式:__________________。请判断改用NaHSO3溶液是否可行?________(填“是”或“否”)。
实验来源于生活且服务于生活,请回答些列问题: (1)正确的实验操作是实验成功的重要因素,下列实验操作错误的是( )
(1)正确的实验操作是实验成功的重要因素,下列实验操作错误的是( )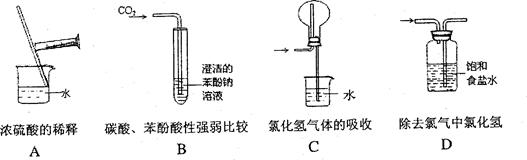
(2)由图的装置中,干燥烧瓶内盛有某种气体,烧杯和滴定管内盛放某种液体。
挤压滴管的胶头,下列与实验事实不相符的是()
A.CO2(NaHCO3溶液)/无色喷泉 B.NH3(H2O含酚酞)/红色喷泉
C.H2S(CuSO4溶液)/黑色喷泉 D.HCl(AgNO3溶液)/白色喷泉
(3)设计学生实验要注意安全、无污染、现象明显。根据启普发生器原理,可用底部有小孔的试管制简易的气体发生器(见右图) 。
。
若关闭K,不能使反应停止,可将试管从烧杯中取出(会有部分气体逸散)。下列气体的制取宜使用该装置的是( )
A.用二氧化锰(粉末)与双氧水制氧气
B.用锌粒与稀硫酸制氢气
C.用碳酸钠固体与盐酸制二氧化碳
D.用碳酸钙(块状)与稀硫酸制二氧化碳
(4)为提纯下列物质(括号内为杂质),选用的试剂和分离方法都正确的是()
| 物质 |
试剂 |
分离方法 |
|
| ① |
硝酸钾(氯化钠) |
蒸馏水 |
重结晶 |
| ② |
二氧化碳(氯化氢) |
饱和碳酸钠溶液 |
洗气 |
| ③ |
乙醇(水) |
生石灰 |
蒸馏 |
| ④ |
苯(苯酚) |
浓溴水 |
分液 |
A.①② B.①③ C.只有③ D.③④
(10分)我国化学家侯德榜(下图所示)改革国外的纯碱生产工艺,生产流程可简要表示如下: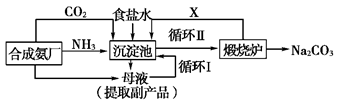
(1)请写出碳酸钠的一种用途 。
(2)写出上述流程中X物质的分子式 。
(3)使原料氯化钠的利用率从70%提高到90%以上,主要是设计了(填上述流程中的编号)的循环,从沉淀池中取出沉淀的操作是 。
(4)该流程中氨气和二氧化碳的添加顺序是:先通氨气后通二氧化碳,请说明理由:。
(12分)某化学兴趣小组在实验室制取漂白粉,并探究氯气与石灰乳反应的条件和产物。已知:①二氧化锰与浓盐酸反应可制备氯气,同时生成MnCl2。②氯气和碱的反应为放热反应。温度较高时,氯气和碱还能发生如下反应:3Cl2+6OH- 5Cl-+ClO3-+3H2O。该兴趣小组设计了下列实验装置,进行实验。
5Cl-+ClO3-+3H2O。该兴趣小组设计了下列实验装置,进行实验。
请回答下列问题:
(1)①甲装置用于制备氯气,其反应的化学方程式是;乙装置的作用是______。
②该兴趣小组用100mL 12mol/L盐酸与 8.7gMnO2制备氯气,并将所得氯气与过量的石灰乳反应,则理论上最多可 制得Ca(ClO)2______________g。
制得Ca(ClO)2______________g。
(2)小组成员发现,产物中Ca(ClO)2的质量明显小于理论值。为了探究反应条件对产物的影响,他们另取一定量的石灰乳,缓慢。匀速地通入足量氯气,得出了ClO-、ClO3-两种离子的物质的量(n)与反应时间(t)的关系曲线,粗略表示为下图(不考虑氯气和水的反应)。①图中曲线I表示_____________离子的物质的量随反应时间变化的关系。
②所取石灰乳中含有Ca(OH)2的物质的量为______________mol。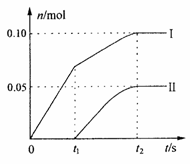
(3)为了提高Ca(ClO)2的产率,可对丙装置作适当改进。请你给出一种改进方法:______。
硫酸工业尾气中二氧化硫含量超过0.05%(体积分数)时需经处理后才能排放。某校兴趣小组欲测定硫酸工业尾气中二氧化硫含量,采用以下方案:
甲方案:如下图所示,图中气体流量计B用于准确测量通过尾气的体积。将尾气通入一定体积已知浓度的碘水中测定二氧化硫的含量。当洗气瓶C中溶液蓝色消失时,立即关闭活塞A,根据碘水用量可计算SO2的量,与气体流量计数据之比即可判断SO2是否超标。
(1)已知二氧化硫与碘水的反应为:SO2+ I2+H2O==H2SO4+HI,配平该反应并指出还原剂。
I2+H2O==H2SO4+HI,配平该反应并指出还原剂。
(2)洗气瓶C中导管末端连接一个多孔球泡D,可以提高实验准确度,其理由是:。
(3)洗气瓶C溶液蓝色消失后,没有及时关闭活塞A,测得的SO2含量
(填“偏高”、“偏低”或“无影响”)。
乙方案:尾气被过氧化氢氧化后与氢氧化钡反应,实验步骤如以下流程图所示:
(4)写出步骤①中反应的化学方程式。
(5)写出步骤②中反应的化学方程式 。
。
(6)通过的尾气体积为VL(已换算成标准状况)时,该尾气中二氧化硫含量(体积分数)为(用含有V、m的代数式表示)。
(7)若将乙方案中步骤①省略,直接将尾气通入过量Ba(OH)2溶液,其余步骤与方案乙相同,你认为这样处理是否合理,说明理由:。
化学能在一定的条件下可以转化为电能。
(一)现有如下两个反应:
① 2FeCl3 + Cu = 2FeCl2 + CuCl2
② Na2CO3 + 2HCl =" 2NaCl" + H2O + CO2↑
(1)根据两个反应的本质判断,您认为可以设计成原电池的是(填反应序号)。
(二)请根据Zn + CuSO4 = ZnSO4 + Cu反应,选择适宜的材料和试剂设计一个 原电池。
原电池。
(2)画出原电池装置图,并在图中标注出电极和电解质溶液的名称。
(3)写出该原电池电极反应式:正极:;负极:。