25℃时,用浓度为0.1000 mol·L-1的NaOH溶液滴定20.00 mL浓度均为0.1000 mol·L-1的三种酸HX、HY、HZ,滴定曲线如下图所示。下列说法正确的是( )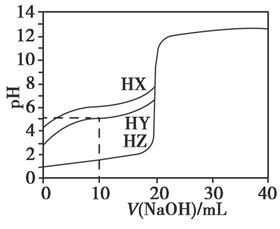
| A.在相同温度下,同浓度的三种酸溶液的导电能力顺序:HZ<HY<HX |
| B.根据滴定曲线,可得Ka(HY)≈10-5 |
| C.将上述HX、HY溶液等体积混合后,用NaOH溶液滴定至HX恰好完全反应时:c(X-)>c(Y-)>c(OH-)>c(H+) |
D.HY与HZ混合,达到平衡时:c(H+)=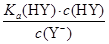 +c(Z-)+c(OH-) +c(Z-)+c(OH-) |
在图中两个相同的容器中分别充入N2(甲容器中)和NO2(乙容器中),在常温常压下,甲、乙两容器的活塞均停在Ⅰ处(图中虚线部分),当用外力缓慢推活塞到Ⅱ处时,外力对容器所做的功的关系是( )
| A.W甲>W乙 | B.W甲<W乙 | C.W甲=W乙 | D.无法比较 |
把镁带投入盛有稀HCl的容器里,产生H2的速率与下列因素有关系的是( )
①盐酸的浓度②温度③镁带的表面积④容器的密闭情况⑤溶液的氯离子浓度
| A.①② | B.③④ | C.①②③④ | D.①②③④⑤ |
一定条件下,在容积为2 L的密闭容器里加入一定物质的量的A,发生如下反应并建立平衡:
A(g) 2B(g),2B(g)
2B(g),2B(g) C(g)+2D(g)
C(g)+2D(g)
测得平衡时各物质的浓度是c(A)="0.3" mol·L-1,c(B)="0.2" mol·L-1,c(C)="0.05" mol·L-1,最初向容器里加入A的物质的量是( )
A.0.5 mol B.0.8 mol C.0.9 mol D.1.2 mol
在两个容积、温度完全相同的甲、乙真空密闭容器中,分别投入1 mol N2,3 mol H2和2 mol N2,6 mol H2,一段时间达到平衡后,甲容器中N2所占体积分数为M%,乙中N2所占体积分数为N%,则M和N正确的关系是( )
| A.M>N | B.M<N | C.M="N" | D.无法比较 |
在一定条件下的密闭容器中,存在如下平衡:
CO2(g)+C(s) 2CO(g)(吸热反应)
2CO(g)(吸热反应)
如果升高温度,气体混合物的平均摩尔质量将会( )
| A.减小 | B.增大 | C.不变 | D.无法判断 |