某同学设计实验以探究元素性质的递变规律,实验装置如图所示。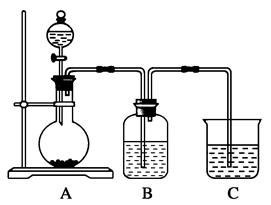
实验Ⅰ:根据元素最高价含氧酸的酸性强弱探究元素非金属性递变规律。
已知A装置的烧瓶里装有大理石,分液漏斗里装有稀HNO3,B装置中装有饱和碳酸氢钠溶液,装置C中装有Na2SiO3溶液,试回答:
(1)A中反应的离子方程式为____________________,C中可观察到的现象是________。
(2)B装置的作用是__________________________________________________________。
(3)根据实验现象推知,碳酸、硝酸、硅酸的酸性强弱顺序是________,由此得出碳、硅、氮三种元素非金属性的强弱顺序是________。
实验Ⅱ:已知常温下高锰酸钾与浓盐酸混合可产生氯气,利用该装置探究氯和溴元素的非金属性强弱。
(4)写出B装置中发生反应的离子方程式:_______________________________________。
(5)C装置的作用是_________________________________________________________。
(6)实验结论:氧化性:____________________,非金属性:____________________。
某化学研究小组在使用FeSO4溶液与NaOH溶液制备Fe(OH)2沉淀过程中观察到生成的白色沉淀迅速转变为灰绿色,最后变为红褐色,该小组针对绿色物质展开研究。
【查阅文献】
| 文献名称 |
有关Fe(OH)2的描述 |
| 《大学普通化学(下册)》 |
白色沉淀,易被氧化成微绿色Fe3(OH)8 |
| 《化学教育》 |
白色沉淀,在冷水中易形成绿色的水合物Fe(OH)2·nH2O,热水中不易形成水合物 |
(1)写出Fe(OH)2在空气中被氧化为Fe(OH)3的化学方程式______________;
【提出假设】假设一:绿色物质是Fe(OH)2·nH2O;
假设二:________________;·······
【实验探究】针对上述假设与假设二,展开实验研究:
| 实验序号 |
实验步骤 |
实验现象 |
| 一 |
①在试管中加入20mL蒸馏水,加热煮沸,滴苯液封 ②保持较高温度,使用长滴管伸入液面下依次挤入一滴饱和FeSO4 溶液、一滴NaOH溶液 |
出现白色絮状沉淀,并能保持一段时间 |
| 二 |
①在试管中加入20mL蒸馏水 ②加入一滴饱和FeSO4 溶液、一滴NaOH溶液 |
出现白色沉淀,迅速转变为灰绿色,最后变为红褐色 |
| 三 |
①在试管中加入20mL蒸馏水,加热煮沸,滴苯液封 ②恢复室温后,使用长滴管伸入液面下依次挤入一滴饱和FeSO4 溶液、一滴NaOH溶液 |
出现白色沉淀,迅速转变为绿色沉淀 |
(1)实验室保存FeSO4溶液常需加入 (填化学式,下同),为检验某FeSO4溶液是否变质,可向溶液中加入______________;
(2)由实验一与实验 (填实验序号)的现象可推断假设 可能成立。
(3)为了进一步探究假设二是否成立,小组成员进行如下实验,请完成下表:
试剂:蒸馏水、NaOH溶液、苯、FeSO4溶液、氧气
| 实验步骤 |
实验现象与结论 |
| ①在试管中加入20mL蒸馏水,加热煮沸,滴苯液封 ② ③ |
若沉淀中出现绿色的迹象,则假设二成立; 若沉淀中没有出现任何绿色的迹象,则假设二不成立。 |
(有机物A可用葡萄发西酵得到,也可从牛奶中提取,纯净的A为无色粘稠液体,易溶于水,为研究A的组成与结构,进行如下实验:
| 实 验 步 骤 |
解 释 或 实 验 结 论 |
| (1)称取A 9.0g,升温使其汽化,测其密度是相同条件下H2的45倍. |
试通过计算填空: (1)A的相对分子质量为:___________ |
| (2)将此9.0g A在足量纯O2充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现分别增重5.4g和13.2g. |
(2)A的分子式为:___________ ____________ |
| (3)另取A 9.0g,跟足量的NaHCO3粉末反应,生成2.24L CO2(标准状况),若与足量金属钠反应则生成2.24L H2(标准状况). |
(3)写出A中所含有的官能团名称:________________ |
(4)A的核磁共振氢谱如图: |
(4)A中含有_____种氢原子. |
| (5)综上所述,A的结构简式___________________ |
实验室采用如下图所示的装置,可将反应粗铜与Cl2反应转化为固体1(部分仪器和夹持装置已略去)。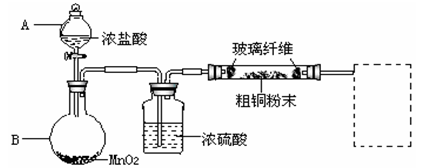
(1)仪器A的名称是 。
(2)连接好装置后,加入药品前,应该进行的实验操作是 。
(3)装置B中发生反应的离子方程式是 。
(4)有同学认为应在浓硫酸洗气瓶前增加吸收HCl的装置,你认为是否必要(填“是”或“否”) 。
(5)虚线内缺少实验装置,请你画出装置图,标明药品名称。
某同学在实验室进行钠的化合物性质的实验。请回答下列问题。
(1)过氧化钠与水反应的化学方程式为 ,实验结束后,向试管所得溶液中滴加酚酞溶液,现是 。
(2)Na2CO3和NaHCO3是两种常见的钠盐。
①下列关于Na2CO3和NaHCO3性质的说法中,正确的是________(填字母)。
a. NaHCO3的俗称是苏打
b. Na2CO3溶液显碱性,说明Na2CO3属于碱
c. 向Na2CO3和NaHCO3固体中分别滴加等浓度的盐酸,后者反应速率快
②按下图所示装置做实验,请回答下列问题。
___________(填“A”或“B”)中澄清石灰水变浑浊,原因是(用化学方程式表示)
________________________________,_________________________________。
某研究性学习小组请你参与“研究铁与水蒸气反应所得固体物质的成分、性质及再利用”实验探究,并共同解答下列问题:
探究一 设计如图所示装置进行“铁与水蒸气反应”的实验。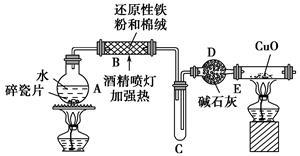
(1)硬质玻璃管B中发生反应的化学方程式为____________________。
(2)反应前A中投放碎瓷片的目的是______________________。
(3)装置E中的现象是___________________________。
探究二 设计如下实验方案确定反应后硬质玻璃管B中黑色固体的成分。
(4)待硬质玻璃管B冷却后,取少许其中的固体物质溶于________后,将所得溶液分成两份。
(5)一份滴加几滴KSCN溶液。若溶液变红色,推断硬质玻璃管B中固体物质的成分为________(选填序号,下同);若溶液未变红色,推断硬质玻璃管B中固体物质的成分为________。
①一定有Fe3O4 ②一定有Fe ③只有Fe3O4 ④只有Fe
探究三 设计如下流程测定反应后硬质玻璃管B中固体含铁元素的质量分数。
|
