为探究某种盐的水解是吸热反应。有四位同学分别设计了如下实验方案:
| 同学 |
实验设计 |
| 甲 |
将硝酸铵晶体溶于水,若水温下降,说明硝酸铵水解是吸热的 |
| 乙 |
加热能使溶液中的Fe3+转化成Fe(OH)3沉淀,说明Fe3+水解是吸热的 |
| 丙 |
通过实验发现同浓度的热的纯碱溶液比冷的纯碱溶液去油污效果好,说明碳酸钠水解是吸热的 |
| 丁 |
在醋酸钠溶液中滴入酚酞试液,加热(不考虑水蒸发)后若红色加深,说明醋酸钠水解是吸热的 |
其中不正确的是( )
A.甲 B.乙 C.丙 D.丁
常温下,取0.2mol/LHX溶液与0.2mol/LNaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=8,则下列说法(或关系式)正确的是()
| A.C(X-)-C(Na+)=9.9×10-7mol/L |
| B.C(Na+)=C(X-)+C(HX)=0.1mol/L |
| C.C(OH-)-C(HX)=C(H+)=1×10-6mol/L |
| D.混合溶液中由水电离出的C(OH-)大于0.2mol/LHX溶液中由水电离出的C(H+) |
下列各项中的两个量,其比例2:1的是( )
| A.硫酸铵固体中n(NH4+)与n(SO42—) |
| B.相同温度下,0.01 mol/L的醋酸溶液与0.02 mol/L 醋酸溶液中的c(H+) |
| C.液面均在“0”刻度时,50 mL酸式滴定管和25 mL酸式滴定管内所盛溶液的体积 |
| D.40℃时pH=7的(NH4)2SO4与NH3·H2O的混合液中,c(NH4+)与c(SO42—) |
比较下列溶液的pH (填“>”、“<”、“=”)
(1)25℃、1mol/LFeCl3溶液_____80℃、1mol/LFeCl3溶液;
(2)0.1mol/L(NH4)2CO3溶液______0.1mol/L Na2CO3溶液。
(3)0.1mol/LNH4Cl溶液______0.01mo1/L NH4Cl溶液;
(4)0.1mol/LNa2CO3溶液______0.1mol/L NaHCO3溶液;
A > < < > B > > > > C < > < > D < < > >
下列离子或分子在溶液中能大量共存,通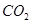 后仍能大量共存的一组是
后仍能大量共存的一组是
A. |
B.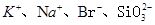 |
C.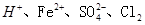 |
D. |
关于浓度均为0.1 mol/L的三种溶液:①氨水、②盐酸、③氯化铵溶液,下列说法不正确的是
A. c(NH4+):③>①
B水电离的氢离子浓度②>①
C.①和②等体积混合后的溶液:c(H+)=c(OH )+c(NH3·H2O)
)+c(NH3·H2O)
D.①和③等体积混合后的溶液呈碱性:c(Cl )>c(NH4+)>c(OH
)>c(NH4+)>c(OH )>c(H+)
)>c(H+)