化学反应A2+B2=2AB的能量变化如图所示,则下列说法正确的是( )
| A.该反应是吸热反应 |
| B.断裂1mol A—A键和1mol B—B键能放出xkJ的能量 |
| C.断裂2mol A—B键需要吸收ykJ的能量 |
| D.2mol AB的总能量高于1 mol A2和1mol B2的总能量 |
一定条件下,在体积为10L的固定容器中发生的反应:N2+3H2 2NH3,反应过程如下图所示,下列说法正确的是
2NH3,反应过程如下图所示,下列说法正确的是
| A.t1 min时正、逆反应速率相等 |
| B.X曲线表示NH3的物质的量随时间变化的关系 |
| C.0~8 min,H2的平均反应速率v(H2)=0.75 mol·L-1·min-1 |
| D.10~12 min,N2的平均反应速率为v(N2)=0.25mol·L-1·min-1 |
一定质量的甲烷燃烧后得到的产物为CO、CO2和水蒸气,此混合气体总质量为49.6g,当其缓慢经过足量无水CaCl2时,无水CaCl2增重25.2g,则原混合气体中CO2的质量为
| A.12.5g | B.13.2g | C.19.7g | D.24.4g |
用于制造隐形飞机的某种物质具有吸收微波的功能,其主要成分的结构如下图,下列说法正确的是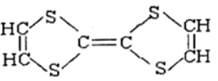
| A.该物质属于烃类 |
| B.该物质易溶于水 |
| C.该物质能使酸性高锰酸钾溶液褪色 |
| D.该物质是一种高分子化合物 |
可逆反应N2+3H2 2NH3的正、逆反应速率可用各反应物或生成物浓度的变化来表示。下列关系中能说明反应已达到平衡状态的是
2NH3的正、逆反应速率可用各反应物或生成物浓度的变化来表示。下列关系中能说明反应已达到平衡状态的是
| A.3v正(N2)=v正(H2) | B.v正(N2)=v逆(NH3) |
| C.2v正(H2)=3v逆(NH3) | D.v正(N2)=3v逆(H2) |
化学反应A2+B2=2AB的能量变化如图所示,则下列说法正确的是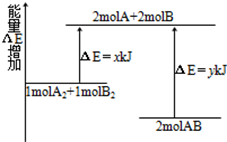
| A.该反应是吸热反应 |
| B.断裂1molA-A键和1molB-B键共放出xkJ能量 |
| C.断裂2molA-B键需要吸收ykJ能量 |
| D.2molAB的总能量高于1molA2和1molB2的总能量 |