有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均用镁片和铝片作电极,但甲同学将电极放入6 mol·L-1的H2SO4溶液中,乙同学将电极放入6 mol·L-1的NaOH溶液中,如图所示。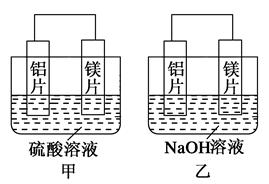
(1)写出甲中正极的电极反应式_____________________________。
(2)乙中负极为________,总反应的离子方程式:
______________________________________________________。
(3)如果甲与乙同学均认为“构成原电池的电极材料如果都是金属,则构成负极材料的金属应比构成正极材料的金属活泼”,则甲会判断出________活动性更强,而乙会判断出________活动性更强。(填写元素符号)
(4)由此实验得出的下列结论中,正确的有________。
| A.利用原电池反应判断金属活动性顺序时应注意选择合适的介质 |
| B.镁的金属性不一定比铝的金属性强 |
| C.该实验说明金属活动性顺序表已过时,没有实用价值了 |
| D.该实验说明化学研究对象复杂、反应受条件影响较大,因此应具体问题具体分析 |
现有pH=2的醋酸溶液甲和pH=2的盐酸乙,请根据下列操作回答问题:
(1)取10mL的甲溶液,加入等体积的水,醋酸的电离平衡_________移动(填“向左”,“向右”或“不”);其pH值变__________(填“增大”、“减小”或“无法确定”);另取10mL的甲溶液,加入少量无水醋酸钠固体(假设加入固体前后,溶液体积保持不变),待固体溶解后,溶液中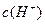 和
和 的比值将____________(填“增大”、“减小”或“无法确定”),其pH值变__________(填“增大”、“减小”或“无法确定”)
的比值将____________(填“增大”、“减小”或“无法确定”),其pH值变__________(填“增大”、“减小”或“无法确定”)
(2)相同条件下,取等体积的甲、乙两溶液,各稀释100倍。稀释后的溶液,其pH大小关系为: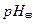 ______
______ (填“大于”、“小于”或“等于”)
(填“大于”、“小于”或“等于”)
(3)各取25mL的甲、乙两溶液,分别用等浓度的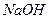 稀溶液中和至
稀溶液中和至 ,则消耗的
,则消耗的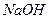 溶液的体积大小关系为:
溶液的体积大小关系为: ______
______ (填“大于”、“小于”或“等于”)
(填“大于”、“小于”或“等于”)
(4)取25mL的甲溶液,加入等体积 的
的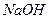 溶液,反应后溶液中
溶液,反应后溶液中 、
、 的大小关系为:
的大小关系为: ______
______ (填“大于”、“小于”或“等于”)
(填“大于”、“小于”或“等于”)
有一种广泛用于汽车、家电产品上的高分子涂料,是按下列流程图生产的。图中M和A都可发生银镜反应,N和M的分子中碳原子数相等,A的烃基上的一氯取代位置有三种。
试写出:
(1)物质的结构简式:A___________,M___________。
(2)反应类型:X____________,Y___________。
(3)物质A的同分异构体结构简式为:___________________________。(写出两个即可)。
(4)D→高分子涂料的化学方程式:___________________________。
(5)N+B→D的化学方程式:___________________________。
有A、B、C、D、E、F、G7瓶不同物质的溶液,它们各是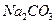 、
、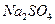 、
、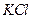 、
、 、
、 、
、 和
和 溶液中的一种。为了鉴别,各取少量溶液进行两两混合,实验结果如表所示。
溶液中的一种。为了鉴别,各取少量溶液进行两两混合,实验结果如表所示。
| A |
B |
C |
D |
E |
F |
G |
|
| A |
- |
- |
- |
- |
- |
- |
↓ |
| B |
- |
- |
- |
- |
↓ |
↓ |
↓ |
| C |
- |
- |
- |
↓ |
- |
↓ |
↓ |
| D |
- |
- |
↓ |
- |
↓ |
↓ |
↓ |
| E |
- |
↓ |
- |
↓ |
- |
↓ |
- |
| F |
- |
↓ |
↓ |
↓ |
↓ |
- |
↓ |
| G |
↓ |
↓ |
↓ |
↓ |
- |
↓ |
- |
表中“↓”表示生成沉淀或微溶化合物,“-”表示观察不到明显变化。试回答下面问题:
(1)A的化学式是_____________,G的化学式是_____________,判断理由是______________________________________________________。
(2)写出其余几种物质的化学式。B:_________,C:_________,D:_________,E_________,F:_________。
以下是元素周期表的示意图,请参照①~⑧在表中的位置,用化学用语回答下列问题:
(1)元素②和⑤的单质和化合物之间在一定条件下存在反应: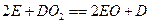 ,其中
,其中 为直线形的非极性分子。
为直线形的非极性分子。 的结构式为_________。
的结构式为_________。
(2)元素③的气态氢化物与最高价氧化物对应的水化物之间可以反应生成盐,该盐在实际生活中的一种用途为___________________________。
(3)元素⑥的单质既能与强酸反应,又能与强碱反应,且元素⑥的单质可以在高温条件下还原三氧化二铁。该反应的化学方程式为___________________________。
(4)由表中两种元素的原子按1:1组成的常见液态化合物的稀溶液易被催化分解,可使用的催化剂为_________(填一种物质的化学式)。
(5)由表中元素形成的常见物质X、Y、Z、M、N可发生如下反应:
①X溶液与Y溶液反应的离子方程式为___________________________。
② ⑥的单质化学方程式为___________________________。
⑥的单质化学方程式为___________________________。
③常温下,为使 溶液中由
溶液中由 电离的阴、阳离子浓度相等,应向溶液中加入一定量的Y溶液至__________________。
电离的阴、阳离子浓度相等,应向溶液中加入一定量的Y溶液至__________________。
一切植物中均含有天然有机高分子化合物A,它是构成植物细胞壁的基础物质,不溶于水,也不溶于一般有机溶剂.能发生如下变化(A~F均分别代表一种物质,框图中的部分产物已略去,如:B生成C的同时还有CO2生成.)
(1)由A生成B化学方程式为.
(2)B、D均含有的官能团是,设计实验,用弱氧化剂检验(1)所得到的溶液中
的B分子结构中存在该官能团(要求:所需仪器和药品可以任选,如需采用实验室不
能长期保存的试剂请写出它的制备过程;以下步骤可以不填满.)
①
②
③
④
(3)从A到F发生的反应类型有.
A.氧化 B.酯化 C.消去 D.水解
(4)写出C到D所发生的化学反应的化学方程式.
(5)F有多种同分异构体,请写出与它有相同官能团的所有同分异构体
.