为了测定乙醇的结构式是 ,利用乙醇和钠的反应,设计如图装置进行实验,在烧瓶中放入足量的钠,从分液漏斗中缓缓滴入一定量的乙醇,通过测量量筒中水的体积,就可知反应生成的氢气的体积。
,利用乙醇和钠的反应,设计如图装置进行实验,在烧瓶中放入足量的钠,从分液漏斗中缓缓滴入一定量的乙醇,通过测量量筒中水的体积,就可知反应生成的氢气的体积。
(1)实验前检验该装置的气密性的实验操作是
__________________________________________________。
(2)有人认为装置中有空气,所测的气体体积应扣除装置中空气的体积,才是氢气的体积,你认为________(填“正确”或“不正确”)。
(3)如果实验开始前b导管内未充满水,则实验结果将________(填“偏大”或“偏小”)。
(4)若测得有1.15 g C2H6O参加反应,把量筒c中的水的体积换算成标准状况下H2的体积为280 mL,试结合计算和讨论,判断下面(Ⅰ)和(Ⅱ)两式中,哪个正确________。
下图是实验室用来验证乙烯与氢气反应产物的装置,请回答下列问题:
(1)此装置用来制取乙烯,其中包括的仪器是:
①碎瓷片②石棉网和铁架台③圆底烧瓶④温度计(量程 100℃)⑤温度计(量程200℃)⑥酒精灯⑦单孔塞⑧双孔塞⑨导管。不选用的仪器有___________(填其序号)
(2)写出实验室制取乙烯的化学方程式 。
(3)此处碱石灰的作用是 。
(4)实验过程中,发现溴水会褪色,可能的原因是 。
(5)装置中点燃的气体刚开始为,出现什么现象可说明生成了乙烷?
实验室制乙烯,常常因为温度过高而使乙醇与浓硫酸反应生成少量的二氧化碳,有人设计下列实验以确认上述混合气体中有乙烯和二氧化硫。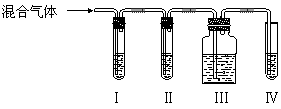
(1)写出实验室制取乙烯的化学方程式________________________________
(2)Ⅰ、Ⅱ、Ⅲ、Ⅳ装置中可盛放的试剂是:(将下列有关试剂的序号填入空格内)
Ⅰ: 、Ⅱ: 、Ⅲ: 、Ⅳ: 。
| A.品红溶液 | B.NaOH溶液 | C.浓硫酸 | D.溴水 |
(3)能说明二氧硫存在的现象是 。
(4)使用装置(Ⅱ)的目的是 。
(5)使用装置(Ⅲ)的目的是 。
(6)确证含乙烯的现象 。
(7)进行下列实验时,都要使用温度计,回答下列问题:
制取乙烯时,温度计水银球部位应放在 。
石油分馏时,温度计水银球部位应放在 。
实验室制备硝基苯的方法是将苯与浓硫酸和浓硝酸的混合液加热到55~60℃反应,已知苯与硝基苯的基本物理性质如下表所示:
| 熔点 |
沸点 |
状态 |
|
| 苯 |
5.51 ℃ |
80.1 ℃ |
液体 |
| 硝基苯 |
5.7 ℃ |
210.9 ℃ |
液体 |
(1)要配制浓硫酸和浓硝酸的混合酸的注意事项是_________。
(2)分离硝基苯和水的混合物的方法是________;分离硝基苯和苯的方法是____________。
(3)某同学用如图装置制取硝基苯: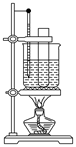
①用水浴加热的优点是_____________________;
②指出该装置的两处缺陷___________________;___________。
实验室制备硝基苯的主要步骤如下:
①配制一定比例的浓硫酸和浓硝酸的混合酸加入反应器中。
②向室温下的混合酸中逐滴加入一定量的苯,充分振荡,混合均匀。
③在50℃~60℃下发生反应。
④除去混合酸后,粗产品依次用蒸馏水和5%的NaOH溶液洗涤,最后用蒸馏水洗涤。
⑤将用无水氯化钙干燥后的粗硝基苯进行蒸馏,得到纯硝基苯。
(1)配制一定比例浓硝酸和浓硫酸混合酸时,操作注意事项是 ;
(2)步骤③的加热方式是 ;
(3)步骤④中,洗涤、分离粗硝基苯应使用的主要玻璃仪器是 ;
(4)步骤④中,粗产品用5%的NaOH溶液洗涤的目的是 ;
(5)纯硝基苯是无色、密度比水 (填“大”或“小”)、具有 气味的油状液体。
(2012年课标1)溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:
按下列合成步骤回答问题:
(1)在a中加入15mL无水苯和少量铁屑,在b中小心加入4.0mL液态溴,向a中滴入几滴溴,有白色烟雾产生,是因为生成了 气体。继续滴加至液溴滴完,装置d的作用是 ;
(2)液溴滴完后,经过下列步骤分析提纯:
①向a中加入10mL水,然后过滤除去未反应的铁屑;
②滤液依次用10mL水、8mL10%的NaOH溶液、10mL水洗涤。NaOH溶液洗涤的作用是 ;
③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤,加入氯化钙的是 ;
(3)经以上分离操作后,粗溴苯中还含有的主要杂质为 ,要进一步提纯,下列操作中必须的是 (填入正确选项前的字母);
A.重结晶B.过滤C.蒸馏D.萃取
(4)在该实验中,a的容积最适合的是 (填入正确选项前的字母)。
A.25mLB.50mLC.250mL D.500mL