下列依据热化学方程式得出的结论正确的是( )
| A.已知2H2(g)+O2(g)=2H2O(g);△H=-483.6 kJ· mol—1则氢气的燃烧热为△H=-241.8 kJ· mol—1 |
| B.已知C(石墨,s)=C(金刚石,s);△H=+1.9kJ·mol-1,可知石墨比金刚石更稳定 |
| C.已知NaOH(ag)+HCl(aq)=NaCl(aq)+H2O(l);△H=-57.4 kJ· mol—1可知:含1mol CH3COOH的溶液与含1mol NaOH的溶液混合,放出热量等于57.4 kJ |
| D.已知2C(s)+2O2(g)=2CO2(g);△H1 2C(s)+O2(g)=2CO(g);△H2,则△H1>△H2 |
如图所示,隔板I固定不动,活塞II可自由移动。M、N两个容器中均发生如下反应:A(g)+3B(g) 2C(g);△H<0。若起始时,M、N容积相同。下列说法正确的是()
2C(g);△H<0。若起始时,M、N容积相同。下列说法正确的是()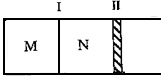
A.起始时,分别向M、N两个容器中加入1molA、1molB,达平衡时,容器M、N中物质A的体积分数相同
B.起始时,分别向M、N两个容器中加入1molA、3molB,达平衡时,容器M中物质A的转化率较大
C.起始时,分别向M、N两个容器中加入2molC,容器N达到平衡所需的时间较短
D.起始时,分别向M、N两个容器中加入1molA、3molB,达到平衡时,容器M中气体的密度较大
下列各组离子,在溶液中能大量共存、加入NaOH溶液后有沉淀生成的一组是()
| A.Fe2+、Ba2+、NO3-、ClO- | B.Ba 2+、NH4+、HCO3-、K+ |
| C.K+、Fe3+、Ba2+、HSO3- | D.Ca2+、HCO3-、NH4+、AlO2- |
将一定量的NaOH和NaHCO3的混合物X放在密闭容器中加热,充分反应后生成V1L气体Z(V1≠0)。反应后的固体残渣Y与过量的稀盐酸反应,又生成V2L气体Z(V1、V2均为标准状况下气体的体积)。下列判断错误的是()
下列实验现象所对应的离子方程式不正确的是()
可逆反应A(g)+3B(g)  2C(g);△H= -QkJ/mol。有甲、乙两个容积相同且不变的密闭容器,向甲容器中加入1molA和3molB,在一定条件下达到平衡时放出热量为Q1kJ;在相同的条件下,向乙容器中加入2molC达到平衡后吸收热量为Q2kJ,已知Q1=3Q2。下列叙述不正确的是()
2C(g);△H= -QkJ/mol。有甲、乙两个容积相同且不变的密闭容器,向甲容器中加入1molA和3molB,在一定条件下达到平衡时放出热量为Q1kJ;在相同的条件下,向乙容器中加入2molC达到平衡后吸收热量为Q2kJ,已知Q1=3Q2。下列叙述不正确的是()
A.甲中A的转化率为75%
B.Q1+Q2=Q
C.达到平衡后,再向乙中加入0.25molA、0.75molB、1.5molC,平衡向正反应方向移动
D.乙中的热化学方程式为2C(g)  A(g)+3B(g);△H= +Q2kJ/mol
A(g)+3B(g);△H= +Q2kJ/mol