铝用来焊接钢轨是利用( )。
| A.铝同氧气反应生成稳定的保护层 |
| B.铝是热的良导体 |
| C.铝是强还原剂,铝热反应放热 |
| D.铝合金强度大 |
已知在25℃,101kPa下,lgC8H18(辛烷)燃烧生成二氧化碳和液态水时放出48.40kJ热量。表示上述反应的热化学方程式正确的是
| A.C8H18(1)+22.5O2(g)=8CO2(g)+9H2O(g)△H=-48.40kJ·mol-1 |
| B.C8H18(1)+22.5O2(g)=8CO2(g)+9H2O(1)△H=-5518kJ·mol-1 |
| C.C8H18(1)+22.5O2(g)=8CO2(g)+9H2O(1)△H=+5518kJ·mol-1 |
| D.C8H18(1)+22.5O2(g)=8CO2(g)+9H2O(1)△H=-48.40kJ·mol-1 |
在1 L密闭容器中,把1 mol A和1 mol B混合发生如下反应:3A(g)+B(g)  xC(g)+2D(g),当反应达到平衡时,生成0.4 mol D,并测得C的平衡浓度为0.4 mol/L,下列叙述中不正确的是
xC(g)+2D(g),当反应达到平衡时,生成0.4 mol D,并测得C的平衡浓度为0.4 mol/L,下列叙述中不正确的是
| A.x的值为2 | B.A的转化率为40% |
| C.B的平衡浓度为0.8 mol/L | D.D的体积分数为20% |
若溶液中由水电离产生的c(OH-)=1×10-14 mol·L-1,满足此条件的溶液中一定可以大量共存的离子组是
| A.Al3+、Na+、NO3-、Cl- | B.K+、Na+、Cl-、NO3- |
| C.K+、Na+、Cl-、AlO2- | D.K+、NH4+、SO42-、NO3- |
铜锌原电池在工作时,下列叙述正确的是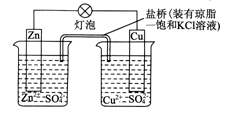
| A.正极反应为:Zn-2e-=Zn2+ |
| B.电池反应为:Zn+Cu2+=Zn2++Cu |
| C.在外电路中,电流从负极流向正极 |
| D.盐桥中的K+移向ZnSO4溶液 |
25℃时,2L pH=13的Ba(OH)2溶液与浓度和它相同的3L NaHSO4溶液混合,反应完全时,生成沉淀的物质的量和此时溶液的pH分别为
| A.0.1mol pH=12 | B.0.02mol pH=2.7 |
| C.0.15mol pH=1 | D.0.3mol pH=10.7 |