(1)在固定体积的密闭容器中通入N2和H2,下列能说明达到平衡的是________。
| A.3v(N2)=v(H2) |
| B.断裂1个N≡N的同时断裂6个N—H |
| C.N2、H2、NH3的物质的量之比是1∶3∶2 |
| D.容器内气体的压强不变 |
E.气体的密度不变
F.气体的平均相对分子质量不变
(2)在2 L的密闭容器中通入2 mol N2、8 mol H2,5 min时达到平衡,测得NH3的物质的量是2 mol,则平衡时c(H2)=______________。
已知2A2(g) + B2(g) 2C(g)
2C(g) 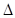 H=" -a" kJ/mol(a>0),在一个有催化剂的固定容积的密闭容器中加入2molA2和1molB2,在500℃是充分反应达到平衡后C的浓度为w mol/L,放出热量b kJ。
H=" -a" kJ/mol(a>0),在一个有催化剂的固定容积的密闭容器中加入2molA2和1molB2,在500℃是充分反应达到平衡后C的浓度为w mol/L,放出热量b kJ。
(1)a b(填“>”“=”或“<”)。
(2)若将反应温度升高到700℃,该反应的平衡常数将 (填“增大”“减小”或“不变”)。
(3)若在原来的容器中,只加入2mol C,500℃时充分反应达到平衡后,吸收热量c kJ,C的浓度 w mol/L(填“>”“=”或“<”),a,b,c之间满足何种关系:
(用等式表示)。
(4)能说明该反应已经达到平衡的状态的是 。
a.ν(C)=2ν(B2) b.容器内压强保持不变
c.ν(A2) (逆) =ν(B2) (正)d.容器内的密度保持不变
氢气是一种新型的绿色能源,又是一种重要的化工原料。
(1)氢气燃烧热值高。实验测得,在常温常压下,1 g H2完全燃烧生成液态水,放出142.9 kJ热量。则H2燃烧热的化学方程式为 。
(2)氢气是合成氨的重要原料,合成氨反应的热化方程式如下:N2(g)+3H2(g) 2NH3(g);ΔH=-92.4 kJ/mol
2NH3(g);ΔH=-92.4 kJ/mol
①当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和NH3的量),反应速率与时间的关系如下图所示。图中t1时引起平衡移动的条件可能是 其中表示平衡混合物中NH3的含量最高的一段时间是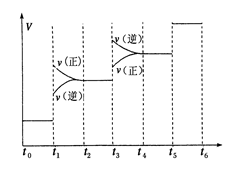
②温度为T ℃时,将2 a mol H2和a mol N2放入0.5 L密闭容器中,充分反应后测得N2的转化率为50%。则反应的平衡常数为
现行中学教材中,有以下化学实验:
A.溴乙烷的水解
B.浓硫酸跟乙醇反应制乙烯
C.乙醛还原新制的氢氧化铜
D.乙酸乙酯的制取
E.石油的蒸馏
F.葡萄糖的银镜反应
G.乙酸乙酯的水解。
对以上实验,按下列各操作的要求,用字母A、B、C、——完成以下填空:(多填扣分)
(1)需用水浴加热的是 ;
(2)实验装置不需要检查气密性的是 ;
(3)为防止液体暴沸,常需加少量碎瓷片的是 ;
(4)需用温度计的是 。
(9分)实验室做乙醛和银氨溶液反应的实验时:
(1)为了得到光亮的银镜,试管应先用 溶液煮沸,倒掉煮沸液体后再用蒸馏水将试管冲洗干净。
(2)配制银氨溶液时向盛有 溶液的试管中逐滴滴加 溶液,边滴边振荡,直到 为止。有关反应的化学方程式为:① ;② 。
(3)加热时应用 加热。产生银镜反应的化学方程式 。
工业上用CO生产燃料甲醇。一定条件下发生反应:CO(g)+2H2(g)  CH3OH(g)。
CH3OH(g)。

(1)图1是表示一定温度下,在体积为2L的密闭容器中加入4mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化情况。从反应开始到平衡,用CO浓度变化表示平均反应速率v(CO)= ; H2的平衡转化率为__________________。
(2)图2表示该反应进行过程中能量的变化。曲线a表示不使用催化剂时反应的能量变化,曲线b表示使用催化剂后的能量变化。写出反应的热化学方程式 。
(3)该温度下,反应平衡常数K=______________(填数值),温度升高,平衡常数K_________(填“增大”、“不变”或“减小”)。
(4)恒容条件下,下列措施中能使反应体系中 增大的措施有 。
增大的措施有 。
a.升高温度b.充入He气
c.再充入2 molH2 d.使用催化剂