铜是重要的金属材料。
(1)工业上可用Cu2S和O2反应制取粗铜,该反应中氧化剂为________。电解粗铜制取精铜,电解时,阳极材料是________,电解液中必须含有的阳离子是________。
(2)在100 mL 18 mol·L-1浓硫酸中加入过量的铜片,加热使之充分反应,反应中被还原的H2SO4为________mol。
(3)电子工业曾用质量分数为30%的FeCl3溶液腐蚀敷有铜箔的绝缘板制印刷电路板,为了从使用过的废腐蚀液中回收铜,并重新得到FeCl3溶液,设计如下实验流程。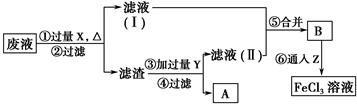
上述流程中,所加试剂的化学式为:X________,Y________,Z________;第⑥步反应的离子方程式为
___________________________________________________。
下列物质中,物质的量最大的是________(填序号,下同),含分子个数最多的是________,含原子个数最多的是________,质量最大的是________。
| A.92 g乙醇(C2H5OH); | B.0.5 mol CO2; | C.148 g H2SO4; |
| D.6 g H2; E.1.204×1024个HCl分子; F.4 ℃时10 mL水 |
100 mL 0.1 mol·L-1 Ba(OH)2溶液与50 mL 0.1 mol·L-1 Na2CO3溶液混合后,边滴边振荡,逐滴加入0.1 mol·L-1 HCl至pH等于7,则需要加入盐酸的体积为_____________mL;如果再加入0.1 mol·L-1酸化的AgNO3溶液至Cl-刚好完全沉淀,则需要加入AgNO3溶液的体积为_____________mL。
用中和滴定的方法测定NaOH和Na2CO3混合溶液中NaOH的含量时,可先在混合溶液中加入过量的氯化钡溶液,使Na2CO3完全变成BaCO3沉淀,然后用标准盐酸滴定(用酚酞作指示剂)。试完成下列问题:
(1)向混有BaCO3沉淀的NaOH溶液中滴入盐酸,为什么不会使BaCO3溶解而能测定NaOH的含量?_______________________________________________________________________。
(2)滴定终点时溶液颜色如何变化?______________________________________________。
(3)滴定时,若滴定管中滴定液一直下降到活塞处才到达终点,能否据此得出准确的滴定结果_______________(填“能”或“不能”)。
(4)能否改用甲基橙作指示剂(填“能”或“不能”) _______________,如果用甲基橙作指示剂,则测定结果如何?_______________(填“偏高”“偏低”或“正确”)。
(1)图Ⅰ表示10 mL量筒中液面的位置,A与B、B与C刻度相差1 mL,如果刻度A为6,量筒中液体的体积是_________mL。
(2)图Ⅱ表示50 mL滴定管中液面的位置,如果液面处的读数是a,则滴定管中液体的体积_________(填字母)。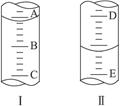
A.a mL B.(50-a) mL C.>a mL D.大于(50-a) mL
(3)若图Ⅰ表示50 mL滴定管中液面位置,A与C刻度间相差1 mL,如果刻度A为6,则液面读数为______________mL。
25 ℃时,若体积为Va、pH=a的某一元强酸与体积为Vb、pH=b的某一元强碱混合,恰好中和,且已知Va<Vb和a=0.5b。请填写下列空白:
(1)a值可否等于3(填“可”或“否”)_________,其理由是___________________________。
(2)a值可否等于5(填“可”或“否”) _________,其理由是___________________________。
(3)a的取值范围是多少?