从绿色化学的理念出发,下列实验不宜用下图所示装置进行的是( )。
| A.不同浓度的硝酸与铜反应 |
| B.稀硫酸与纯碱或小苏打反应 |
| C.铝与氢氧化钠溶液或盐酸反应 |
| D.H2O2在不同催化剂作用下分解 |
某溶液中含有NO3-、CH3COO-、S2-、SO32-等四种阴离子,若向其中加入过量的盐酸溶液,搅拌后再加入过量的NaOH溶液,溶液中没有减少的离子是()
| A.NO3- | B.CH3COO- | C.S2- | D.SO32- |
在自然界中的矿物中,CuSO4可将FeS2氧化,生成Cu2S、SO42-和Fe2+。下列表示该反应的离子方程式中,正确的是()
| A.14Cu2++5S22-+12H2O=7Cu2S+3SO42-+24H+ |
| B.14Cu2++5FeS2+28OH-=7Cu2S+3SO42-+5Fe2++14H2O |
| C.14Cu2+ +5FeS2+24OH-=7Cu2S+3SO42-+5Fe2++12H2O |
| D.14Cu2++5FeS2+12H2O=7Cu2S+3SO42-+5Fe2++24H+ |
已知-CH2CH2CH3称为丙基,-CH(CH3)2称为异丙基。用系统命名法给下列烷烃命名,正确的是()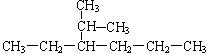
| A.3-异丙基己烷 | B.2-甲基-3-丙基戊烷 |
| C.2-甲基-3-乙基己烷 | D.1,1-二甲基-2-乙基戊烷 |
下图表示的是某离子X的水解过程示意图,则离子X可能是()
| A.CO32- | B.HCO3- | C.Na+ | D.NH4+ |
将某弱酸HA amol与其盐NaA bmol溶于水配成混合溶液,已知该混合溶液中c(H+)+c(HA)=c(Na+)+c(OH-),则对该溶液的分析错误的是()
A.若c(H+)>c(OH-),则c(A-) >c(HA)
B.若c(H+)<c(OH-),则c(HA) >c(A-)
C.a>b
D.a=b