“绿色化学”是人们最近提出的一个新概念,主要内容之一是指从技术、经济上设计可行的化学反应,尽可能减少对环境的副作用,下列化学反应符合绿色化学概念的是( )。
| A.制CuSO4:Cu+2H2SO4(浓)=CuSO4+SO2↑+2H2O |
| B.制CuSO4:2Cu+O2=2CuO,CuO+H2SO4(稀)=CuSO4+H2O |
| C.制Cu(NO3)2:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O |
| D.制Cu(NO3)2:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O |
在一个固定容积的密闭容器中,可发生以下反应:A(g)+B(g)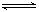 xC(g);∆H=?符合下图(a)所示的关系w(c)为C的质量分数,由此推断关于图(b)的说法正确的是
xC(g);∆H=?符合下图(a)所示的关系w(c)为C的质量分数,由此推断关于图(b)的说法正确的是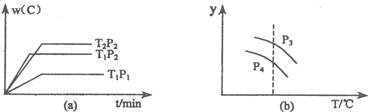
| A.P3>P4,y轴表示A的转化率 |
| B.P3<P4,y轴表示B的体积分数 |
| C.P3<P4,y轴表示混合气体的平均相对分子质量 |
| D.P3>P4,y轴表示混合气体的密度 |
对恒温恒容密闭容器中的可逆反应:A(g)+3B(g) 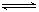 2C(g) ∆H <0,下列叙述错误的是
2C(g) ∆H <0,下列叙述错误的是
| A.升高温度v(正)、v(逆)都增大,但v(逆)增的更大 |
| B.增大压强v(正)、v(逆)都增大,但v(正)增的更大 |
| C.增大A的浓度v(正)会增大,但v(逆)会减小 |
| D.采用正的催化剂一般v(正)、v(逆)同时增大,而且增大的倍数相同 |
下列说法中正确的是
| A.升高温度只能加快吸热反应速率 |
| B.对于任何反应,增大压强都可加快反应速率 |
| C.用正催化剂只能加快正反应速率 |
| D.使用催化剂可同时改变正逆反应速率 |
对反应4A+5B=4C+6D,以下化学反应速率的表示中,所表示反应速率最快的是
A. v (A)=0.40mol•L-1•s-1
B. v (B)=0.48mol•L-1•s-1
C. v (C)=0.36mol•L-1•s-1
D. v (D)=0.55mol•L-1•s-1
反应4A(g )+3B(g)=2C(g)+D(g),经2min,B的浓度减少0.6 mol•L-1。对此反应速率的表示,正确的是
①用A表示的反应速率是0.4 mol•L-1•min-1
②分别用B、C、D表示的反应速率其比值为3:2:1
③在2 min末的反应速率,用B表示是0.3 mol•L-1•min-1
④在这2 min内用B表示的反应速率的值是逐渐减小的,用C表示的反应速率的值是逐渐增大的
A. ①②
B. ③
C. ①
D. ②④