分析以下两个案例,回答后面问题。
(1)某城镇生产、生活的分布情况如图所示,河流中W、X、Y、Z处某次水样抽测结果如表所示。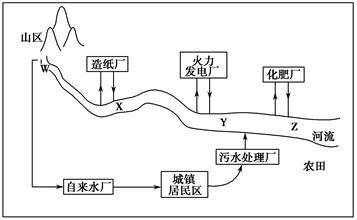
| 地点 项目 |
W |
X |
Y |
Z |
| 水温/℃ |
15 |
18 |
26 |
25 |
| pH |
6 |
8 |
5 |
5 |
| 溶解氧量/(mg·L-1) |
11 |
9 |
7 |
3 |
①导致X、Y处水样pH变化的原因可能是______________________________;
②Z处鱼类大量减少,产生这种现象的原因可能是_________________________。
(2)某地区已探明蕴藏有丰富的赤铁矿(主要成分为Fe2O3、还含有SiO2等杂质)、煤矿、石灰石和黏土。拟在该地区建设大型炼铁厂。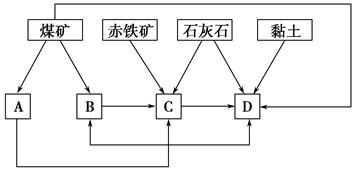
①随着铁矿的开发和炼铁厂的建立,需要在该地区相应建立焦化厂、发电厂、水泥厂等,形成规模的工业体系。据此确定上图中相应工厂的名称A________、B________、C________、D________;
②以赤铁矿为原料,写出高炉炼铁中得到生铁和产生炉渣的化学方程式_____________________________________________________________;
③从“三废”利用、环境保护等角度考虑,该地区和企业在生产中应采取的一些措施有____________(列举2种即可)。
取出的10mL溶液中,AlO2-的物质的量浓度为;
样品中Al的质量分数为(用小数表示,小数点后保留两位)。
该小组为了测定其中Al2O3的含量,从上面反应后的100mL溶液中,取出10mL溶液,逐滴加入1mol/L的盐酸,当滴到5.00mL时开始产生沉淀,继续滴加盐酸,至25.00mL时沉淀恰好全部溶解。
反应中产生的H2质量为___________________ g。
(本题共10分)
某实验小组利用如下图装置,测定某种旧铝合金(含Al2O3和其它不溶于NaOH溶液的成分)中Al的质量分数,其中100mLNaOH溶液过量,每隔相同时间读得电子天平的数据如下表: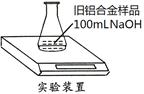
| 称量对象 |
读数次数 |
质量(g) |
| 样品 |
第1次 |
2.582 |
| 锥形瓶+100mL NaOH溶液 |
第2次 |
185.721 |
| 锥形瓶+NaOH溶液+样品 |
第3次 |
188. 286 |
| 第4次 |
188. 254 |
|
| 第5次 |
188. 243 |
|
| 第6次 |
188. 243 |
52.反应的化学方程式为。
第三组学生进行了两次滴定,消耗标准盐酸体积的数据如下表,其中第2次滴定后滴定管的读数如右图所示,将这一读数填入表中。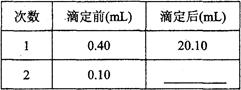

该组学生所测得的烧碱样品中NaOH的质量分数为__________________。