已知:
—C≡CH+—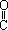 —H
—H —C≡C—
—C≡C—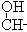
以乙炔为原料,通过下图所示步骤能合成有机中间体E(转化过程中的反应条件及部分产物已略去)。
C2H2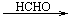 A
A B
B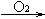 C
C D
D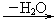 E:H—
E:H—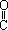
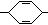
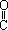 —H
—H
其中,A、B、C、D分别代表一种有机物,B的化学式为C4H10O2,分子中无甲基。
请回答下列问题:
(1)A生成B的化学反应类型是_________________。
(2)写出生成A的化学反应方程式_________________________________________。
(3)B在浓硫酸催化下加热,可生成多种有机产物。写出2种相对分子质量比A小
的有机产物的结构简式:_________________、__________________。
(4)写出C生成D的化学反应方程式:
__________________________________________________________________。
(5)含有苯环,且与E互为同分异构体的酯有______种,写出其中一种同分异构体
的结构简式___________________________________。
已知A、B、C、D和E 5种分子所含原子数目依次为1、2、3、4和6,且都含有18个电子。又知B、C和D是由两种元素的原子组成。请回答:
(1)组成A分子的原子的核外电子排布式是;
(2)B和C的分子式分别是和;C分子的立体结构呈型,该分子属于分子(填“极性”或“非极性”);
(3)若向D的稀溶液中加入少量二氧化锰,有无色气体生成。则D的分子式是,该反应的化学方程式为;
(4)若将1mol E在氧气中完全燃烧,只生成1mol CO2和2molH2O,则E的分子式是。
1919年,Langmuir提出等电子原理:原子数相同、电子总数相同的分子,互称为等电子体。等电子体的结构相似、物理性质相近。
(1)根据上述原理,仅由第2周期元素组成的共价分子中,互为等电子体的是:和;和。
(2)此后,等电子原理又有所发展。例如,由短周期元素组成的微粒,只要其原子数相同,各原子最外层电子数之和相同,也可互称为等电子体,它们也具有相似的结构特征。在短周期元素组成的物质中,与NO2—互为等电子体的分子有:、。
用A+、B-、C2-、D、E、F、G和H分别表示含有18个电子的八种微粒(离子或分子),请回答:
(1)A元素是_______、B元素是_______、C元素是_______(用元素符号表示)。
(2)D是由两种元素组成的双原子分子,其分子式是__________。
(3)E是所有含18个电子的微粒中氧化能力最强的分子,其分子式是__________。
(4)F是由两种元素组成的三原子分子,其分子式是_______,电子式是__ ______。
(5)G分子中含有4个原子,其分子式是__________。
(6)H分子中含有8个原子,其分子式是__________。
黄铁矿(主要成分为FeS2)是工业制取硫酸的重要原料,其煅烧产物为SO2和Fe3O4。(1)将0.050molSO2(g)和0.030molO2(g)放入容积为1L的密闭容器中,反应:2SO2(g)+O2(g)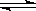 2SO3(g)在一定条件下达到平衡,测得c(SO3)=0.040mol/L。计算该条件下反应的平衡常数K和SO2的平衡转化率(写出计算过程)。
2SO3(g)在一定条件下达到平衡,测得c(SO3)=0.040mol/L。计算该条件下反应的平衡常数K和SO2的平衡转化率(写出计算过程)。
(2)已知上述反应是放热反应,当该反应处于平衡状态时,在体积不变的条件下,下列措施中有利于提高SO2平衡转化率的有 (填字母)
A升高温度 B降低温度 C增大压强
D减小压强 E加入催化剂 G移出氧气
(3)SO2尾气用饱和Na2SO3溶液吸收可得到更要的化工原料,反应的化学方程式为
。
(4)将黄铁矿的煅烧产物Fe3O4溶于H2SO4后,加入铁粉,可制备FeSO4。酸溶过程中需保持溶液足够酸性,其原因是 。
[思路分析]本试题考查“起”、“转”、“平”三步骤计算方法和平衡常数计算方法。
2005年3月29日,由山东开往上海的载有35吨液氯的槽罐车,行驶到了京沪高速公路淮安段,突然翻倒而发生泄漏事故。两天之内造成公路旁的三百多村民入院抢救,其中二十多人中毒死亡的特大伤亡事故。为了防止氯气进一步泄漏,抢险技术人员决定就近采用化学方法处理。将液氯罐吊入离现场200米处的人工水塘中。除在池里注入大量的水外还按比例注入稍过量的某化学物质A的溶液,使氯气快速与之反应,最终事故得以控制。根据上述事实和相关的化学知识,回答下列问题:
(1)槽罐车翻倒而发生泄漏时,可以观察到的现象是;在事发中心地点可采用的防护方法是()
A.人、畜应躲到低洼的地方 B.人、畜应到较高的地方
C.可用盐酸浸湿的软布蒙面 D.人、畜在撤离时,应逆风而行
(2)将泄漏的液氯罐淹没到人工水塘中,观察到池塘里的“水”呈色,其中含有的物质有(填化学式);注入稍过量物质A的溶液,观察到池塘里的“水”的颜色变化是,反应的化学方程式为。
(3)液氯发生泄漏弥漫在空气当中之后,大片的庄稼和树木都由绿变黄全都被“烧死”。植物被“烧死”的原因是;液氯的泄漏也使方圆数十平方公里的土壤被污染,改良土壤可施用一种建筑工业及化工生产中常用的物质B。则B物质是(填化学式),在土壤改良的过程中可适当种植芒萁、岗松、茶花和杜鹃等植物,则这些植物适宜在(填酸性、碱性或中性)土壤。