下述根据下列操作和现象,所得结论正确的是
| |
实验操作及现象 |
实验结论 |
| A |
分别向2 mL 0.1 mol·L-1 CH3COOH溶液和2 mL 0.1 mol·L-1 H3BO3溶液中滴加等浓度的NaHCO3溶液,前者有气泡产生,后者无明显现象 |
酸性: CH3COOH > H2CO3> H3BO3 |
| B |
向2 mL 0.1 mol·L-1 NaOH溶液中滴加3滴0.1 mol·L-1 MgCl2溶液,出现白色沉淀后,再滴加3滴0.1 mol·L-1 FeCl3溶液,出现红褐色沉淀 |
溶解度:Mg(OH)2>Fe(OH)3 |
| C |
在少量无水乙醇中加入金属Na,生成可以在空气中燃烧的气体 |
CH3CH2OH是弱电解质 |
| D |
用3 mL稀H2SO4溶液与足量Zn反应,当气泡稀少时,加入 1 mL浓H2SO4,又迅速产生较多气泡 |
H2SO4浓度增大,反应速率加快 |
下列表示对应化学反应的离子方程式正确的是
A.MnO2与浓盐酸反应制Cl2:MnO2+4HCl Mn2++2Cl-+Cl2↑+2H2O Mn2++2Cl-+Cl2↑+2H2O |
| B.明矾溶于水产生Al(OH)3胶体:Al3++3H2O=Al(OH)3↓+3H+ |
| C.Na2O2溶于水产生O2:Na2O2+H2O=2Na++2OH-+O2↑ |
| D.Ca(HCO3)2溶液与少量NaOH溶液反应:HCO3-+Ca2++OH-=CaCO3↓+H2O |
下列离子或分子在溶液中能大量共存,通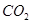 后仍能大量共存的一组是
后仍能大量共存的一组是
A. |
B.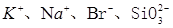 |
C. |
D.K+、Ag+、NH3*H2O、NO3- |
已知下列分子或离子在酸性条件下都能氧化KI,自身发生如下变化:
H2O2→H2O IO3-→I2 MnO4-→Mn2+ HNO2→NO
如果分别用等物质的量的这些物质氧化足量的KI,得到I2最多的是 ( )
| A.H2O2 | B.IO3- | C.MnO4- | D.HNO2 |
物质氧化性、还原性的强弱,不仅与物质的结构有关,还与物质的浓度和反应温度等有关。下列各组物质:①Cu与HNO3溶液 ②Cu与FeCl3溶液 ③Zn与H2SO4溶液 ④Fe与HCl溶液由于浓度不同而发生不同氧化还原反应的是 ()
| A.①③ | B.③④ | C.①② | D.①③④ |
下列关于胶体的叙述不正确的是()
| A.胶体区别于其他分散系的本质特征是分散质的微粒直径在10-9 ~ 10-7m之间 |
| B.光线透过胶体时,胶体中可发生丁达尔效应 |
| C.用平行光照射NaCl溶液和Fe(OH)3胶体时,产生的现象相同 |
| D.Fe(OH)3胶体能够使水中悬浮的固体颗粒沉降,达到净水目的 |