用NA表示阿伏加德罗常数的数值,下列说法正确的是
| A.46 g NO2和N2O4的混合物中含有的氮原子数为NA |
| B.常温常压下,22.4L乙烯中含极性共价键数目为5NA |
| C.1 L 0.1 mol/L的Fe2(SO4)3溶液中,Fe3+的数目为0.2 NA |
| D.1 mol羟基(—OH)中含电子数为10 NA |
将一定量的Fe和Fe2O3的混合物放入250 mL、1.8 mol·L-1的HNO3溶液中,当固体混合物完全溶解后,在标准状况下生成1.12 L NO(HNO3的还原产物仅此一种),再向反应后的溶液中加入1.0 mol·L-1 NaOH溶液,若要使铁元素完全沉淀,所加入的NaOH溶液的体积最少应为( )
| A.300 mL | B.400 mL | C.450 mL | D.500 mL |
已知NaCN溶液呈碱性,(CN)2与卤素单质的性质相似,CN-的还原性介于Br-、I-之间。下列变化不能发生的是( )
A.HCN H++CN- H++CN- |
| B.(CN)2+CH2=CH2―→NC—CH2—CH2—CN |
| C.(CN)2+2Br-=2CN-+Br2 |
| D.(CN)2+2OH-=CN-+CNO-+H2O |
金属钛(Ti)性能优越,被称为继铁、铝后的“第三金属”。工业上以金红石为原料制取Ti的反应为
aTiO2+bCl2+cC aTiCl4+cCO反应(1)
aTiCl4+cCO反应(1)
TiCl4+2Mg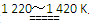 Ti+2MgCl2反应(2)
Ti+2MgCl2反应(2)
关于反应(1)、(2)的分析不正确的是( )
①TiCl4在反应(1)中是还原产物,在反应(2)中是氧化剂;
②C、Mg在反应中均为还原剂,被还原;
③在反应(1)、(2)中的还原性C>TiCl4,Mg>Ti;
④a=1,b=c=2;
⑤每生成19.2 g Ti(Mr=48),反应(1)、(2)中共转移4.8 mol e-。
A.①②④ B.②③④ C.③④ D.②⑤
a mol FeS与b mol Fe3O4投入到V L c mol·L-1的硝酸溶液中恰好完全反应,假设只产生NO气体。所得澄清溶液的成分是Fe(NO3)3和H2SO4的混合液,则反应中未被还原的硝酸为( )
| A.(a+3b) mol | B.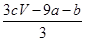 mol mol |
C. mol mol |
D.(cV-3a-9b) mol |
ClO2是一种杀菌消毒效率高的水处理剂,实验室可通过以下反应制得:2KClO3+H2C2O4+H2SO4=2ClO2↑+K2SO4+2CO2↑+2H2O。下列说法中不正确的是( )
| A.ClO2是还原产物 |
| B.1 mol KClO3参加反应,失去电子为1 mol |
| C.H2C2O4在反应中被氧化 |
| D.H2C2O4的还原性大于ClO2的还原性 |