已知:①Na3N+3H2O=3NaOH+NH3↑,②NaH+H2O=NaOH+H2↑。下列叙述正确的是
| A.离子半径:Na+>N3->H+ |
| B.反应①和②都是氧化还原反应 |
| C.反应②每生成1 mol H2,转移的电子数为NA |
| D.Na3N和NaH与盐酸反应都只生成一种盐 |
如图为某有机物的结构简式。已知酯类在铜铬氧化物(CuO·CuCrO4)催化下,与氢气反应得到醇,羰基双键可同时被还原,但苯环在催化氢化过程中不变,其反应原理如下: 

关于该化合物的下列说法中,不正确的是
| A.该有机物的化学式为C20H14O5 |
| B.该有机物可以与浓溴水反应 |
| C.与足量氢氧化钠溶液充分反应,所得产物中有醇类物质 |
| D.1mol该有机物在铜铬氧化物催化下仅能与2mol氢气发生反应 |
为了研究在温度对苯催化加氢的影响,以检验新型镍催化剂的性能。采用相同的微型反应装置,压强为0.78Mpa,氢气、苯的物质的量之比为6.5:1。定时取样分离出氢气后,分析成分得如下表结果:
| 温度/℃ |
85 |
95 |
100 |
110~240 |
280 |
300 |
340 |
|
| 质量分数(%) |
苯 |
96.05 |
91.55 |
80.85 |
0 |
23.35 |
36.90 |
72.37 |
| 环己烷 |
3.95 |
8.45 |
19.15 |
100 |
76.65 |
63.10 |
27.63 |
下列说法错误的是
| A.当温度超过280℃,苯的转化率迅速下降,可能是因为该反应为吸热的可逆反应 |
| B.在110~240℃苯的转化率为100%。说明该镍催化剂活性较高,能够在较宽的温度范围内催化而且不发生副反应 |
| C.增大压强与提高氢气、苯的物质的量比都有利于提高苯的转化率 |
| D.由表中数据来看,随着反应温度的升高,苯的转化率先升高后降低 |
下列反应的离子方程式不正确的是
| A.等体积、等物质量浓度的Ca(H2PO4)2溶液与NaOH溶液混合:Ca2++H2PO4-+OH- ="=" CaHPO4↓+H2O |
| B.过量二氧化碳通入偏铝酸钠溶液中:CO2+2H2O+AlO2-=Al(OH)3↓+HCO3- |
| C.在溶液中亚硫酸氢铵与等物质的量氢氧化钠混合:NH4++HSO3-+2OH-=SO32-+NH3↑+2H2O |
| D.碳酸氢镁溶液中加入过量石灰水:Mg2++2HCO3-+2Ca2++4OH-=2CaCO3↓+Mg(OH)2↓+2H2O |
用NA表示阿伏加德罗常数的值,下列说法中正确的是
| A.100mL 1mol·L-1 FeCl3溶液中含阳离子数为0.1NA |
| B.标准状况下,2.24 L乙醛完全燃烧所得CO2分子数为0.2NA |
| C.0.6 g CaCO3与Mg3N2的混合物中所含质子数为0.3NA |
| D.80 mL 10 mol·L-1浓盐酸与足量MnO2反应,转移电子数为0.4NA |
下列说法你认为不正确的是
A.实验室从苯酚中分离出苯的过程中,可选用右图装置及操作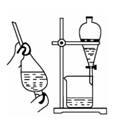 |
| B.化学反应中原子可重新组合、也可以破裂,爆炸过程中不一定伴随着化学反应 |
| C.大气中的氮气可通过生物固氮、自然固氮和工业固氮等方式从游离态转变为化合态,氮的固定过程中必定发生氧化还原反应 |
| D.化学家合成和分离了超过4500万种物质基础。化学合成和分离技术为信息技术、生物技术、航空航天技术等奠定了物质基础 |